
Хирургическое лечение каверном полушарий большого мозга. Анализ ближайших и отдаленных результатов лечения. Диссертация на соискание ученой степени кандидата медицинских наук

Хирургическое лечение каверном полушарий большого мозга. Анализ ближайших и отдаленных результатов лечения
Диссертация на соискание ученой степени кандидата медицинских наук
Дмитрий Николаевич Окишев
© Дмитрий Николаевич Окишев, 2016
ISBN 978-5-4483-3412-2
Создано в интеллектуальной издательской системе Ridero
РОССИЙСКАЯ АКАДЕМИЯ МЕДИЦИНСКИХ НАУК
Федеральное государственное бюджетное учреждение
«Научно-исследовательский институт нейрохирургии имени академика Н. Н. Бурденко»
ОКИШЕВ ДМИТРИЙ НИКОЛАЕВИЧ
Хирургическое лечение каверном полушарий
большого мозга. Анализ ближайших и отдаленных результатов лечения
Специальность: 14.01.18 – нейрохирургия
Диссертация на соискание ученой степени кандидата медицинских наук
Научные руководители:
профессор, д.м. н. Элиава Ш. Ш.
д.м. н. Белоусова О. Б.
Москва 2012
Список сокращений
АВМ – артерио-венозная мальформация
АГ – ангиография
АД – артериальное давление
ЗМА – задняя мозговая артерия
ЗЧЯ – задняя черепная ямка
КТ – компьютерная томография
ЛП – люмбальная пункция
МР – магнитно-резонансный
МРТ – магнитно-резонансная томография
НИИ – научно-исследовательский институт
ПВА – передняя ворсинчатая артерия
ПМА – передняя мозговая артерия
САК – субарахноидальное кровоизлияние
СМА – средняя мозговая артерия
ТМО – твердая мозговая оболочка
ЦНС – центральная нервная система
ЭКоГ – электрокортикография
ЭЭГ – электроэнцефалография
Введение. Актуальность темы
Среди пациентов, обращающихся к нейрохирургу за консультацией в связи с установленным диагнозом «кавернома» полушарий большого мозга, можно выделить две основные группы. Первая представлена больными, у которых кавернома проявилась клинически в виде эпилептических припадков или типичной картины внутричерепного кровоизлияния. Вторую группу составляют пациенты, у которых кавернома явилась случайной находкой. Как правило, в последней группе патология выявляется при обследовании по поводу какого-либо другого заболевания, либо в связи с минимальными неспецифическими жалобами (чаще всего, головной болью). Ко второй группе часто относятся кровные родственники больных с каверномами, принявшие решение провести обследование для исключения наследственной патологии. Число пациентов обеих групп неуклонно возрастает, что связано, в первую очередь, с широким внедрением методов нейровизуализации. При этом происходит постепенное смещение в сторону больных с коротким анамнезом и минимальными клиническими проявлениями заболевания, либо их отсутствием. Улучшение качества нейровизуализации привело также к увеличению числа больных с небольшими мальформациями, размеры которых не превышают 1 см, а также с множественными каверномами. Все эти случаи требуют от нейрохирурга принятия решения о тактике ведения, и, в первую очередь, решения вопроса о показаниях и противопоказаниях к хирургическому вмешательству с целью удаления каверном.
К концу 20-го века был накоплен значительный опыт и сформулированы основные принципы лечения каверном головного мозга. Этот опыт основан, главным образом, на результатах лечения больных с четко очерченными клиническими формами заболевания. Необходимость принятия решения о тактике ведения больных с каверномами, морфологические и клинические проявления которых отличаются от «классических» форм заболевания, с одной стороны, и совершенствование микрохирургической техники и появление различных интраоперационных методов визуализации и контроля, с другой, заставляют пересматривать и уточнять как показания к операциям, так и методику их выполнения.
С учетом того, что каверномы, как правило, характеризуются доброкачественным течением, определение показаний к операции является трудной задачей и зависит от многих факторов. Решение этого вопроса является особенно сложным при неопределенных клинических проявлениях заболевания, редких эпилептических припадках и эпилепсии, хорошо поддающейся противосудорожной терапии. В ряде клиник в подобных случаях делается выбор в пользу консервативного лечения больных. При доказанных кровоизлияниях из каверном решение об операции становится более определенным, однако и в этих случаях оно не является однозначным, особенно при каверномах, расположенных в глубинных и функционально важных зонах мозга. В пользу операции свидетельствуют данные о высокой эффективности хирургического лечения эпилепсии, а также тот факт, что эффективность лечения припадков после операции находится в обратной зависимости от продолжительности эпилептического анамнеза.
Помимо клинических проявлений, важным в определении тактики лечения больных является оценка анатомических и гистологических особенностей каверном.
В настоящее время не существует четко сформулированных показаний и противопоказаний к хирургическому лечению каверном, в связи с чем каждая клиника самостоятельно их формирует, основываясь на результатах лечения больных в других крупных центрах и исходя из собственных данных. Опыт хирургического лечения каверном различной локализации в НИИ нейрохирургии к настоящему времени составляют около 600 больных, оперированных по поводу данной патологии. Подавляющее большинство из этих вмешательств выполнены у больных с каверномами полушарий большого мозга. В то же время, анализ операций при супратенториальных каверномах ограничивается работами Амиридзе Н. Ш., обобщившей результаты лечения 50 больных за 1971—1992 гг. [1], и Белоусовой О. Б., проанализировавшей результаты хирургического и консервативного лечения 160 больных за 1992—2002 гг. [2].
Произошедшие за последние годы изменения в диагностических возможностях, появление новых интраоперационных методик, значительное увеличение количества выполняемых операций обосновывают необходимость дальнейшего анализа результатов лечения, что позволит выработать наиболее оптимальные подходы к ведению таких больных на современном этапе.
Цель исследования
Уточнение показаний к хирургическому лечению каверном полушарий большого мозга.
Задачи исследования
Оценить возможности современных пред- и интраоперационных инструментальных вспомогательных методик в улучшении качества хирургического лечения каверном и функциональных исходов операций. Оценить необходимость их использования в зависимости от топографо-анатомических особенностей каверномы и клинических проявлений заболевания.
Оценить ближайшие результаты хирургического лечения каверном. Проанализировать интра- и послеоперационные осложнения.
Оценить отдаленные результаты хирургического лечения каверном.
Проанализировать значимость факторов, влияющих на неврологический и эпилептологический исход лечения.
Научная новизна исследования
Впервые на значительном материале института нейрохирургии им. акад. Н. Н. Бурденко проанализированы ближайшие результаты хирургического лечения каверном полушарий большого мозга. На основании данных катамнеза оценены отдаленные результаты хирургического лечения и факторы, влияющие на курабельность эпилептического синдрома. Также выполнена оценка возможностей современных пред- и интраоперационных инструментальных вспомогательных методик в улучшении качества хирургического лечения каверном и функциональных исходов операций.
Практическая значимость
Результаты работы позволили уточнить показания и противопоказания к хирургии каверном полушарий большого мозга, улучшить диагностику и результаты лечения каверном. Работа может быть использована для улучшения оказания медицинской помощи в других клиниках нашей страны.
Глава 1. Современное состояние проблемы хирургического лечения каверном полушарий большого мозга
1.1 Историческая справка
Первой публикацией, в которой встречается описание сосудистой мальформации ЦНС, является работа У. Гунтера, опубликованная в 1757 г. – «Observation on arteriovenous malformations» [137]. В ней впервые использован термин «мальформация». В двух фундаментальных работах, опубликованных в 6-м томе Вирховского Архива в 1854 г., анатомом Х. Люшкой и самим Р. Вирховым были обобщены все сведения о сосудистых опухолях и аномалиях, накопленные к тому моменту. Авторы выделяют телеангиоэктазии и кавернозные ангиомы (собственно термин «кавернозная ангиома» впервые использован Rokitansky для описания образований вне ЦНС [32]). Каверномы были первоначально отнесены к опухолям. Вирхов относил их к истинным опухолям, в отличие от телеангиоэктазий. В более поздней работе, написанной в 1863 г. Вирхов вновь проводит анализ сосудистых аномалий и относит каверномы к порокам развития [127]. Среди сосудистых мальформаций он выделял простую ангиому (куда относил телеангиоэктазии), кавернозную ангиому, группу рацемозных ангиом (артериальный, венозный и артериовенозный варианты) и лимфангиому. Об удалении каверномы впервые сообщено Bermer и Carson в 1890 году [99]. В работах начала XX века кавернома уже, как правило, описывается как отдельная форма сосудистых мальформаций. Первая обзорная работа на данную тему выполнена Dandy в 1928 году [32]. Автор представил 5 своих наблюдений и проанализировал 44 случая, опубликованных в литературе. В работе описаны типичные клинические проявления, техника удаления каверном. Спустя 8 лет Bergstrandt и соавт. опубликовали большую работу по результатам лечения нейроваскулярной патологии в Каролинском медицинском университете (Стокгольм), в которой в частности выполнен обзор данных по хирургическому лечению каверном ЦНС и предложен ряд диагностических критериев для каверном ЦНС [18]. В 1966 McCormik публикует практически не изменившуюся до настоящего времени классификацию сосудистых мальформаций, в которой выделено 4 типа образований: капиллярные телеангиоэктазии, венозные ангиомы, кавернозные ангиомы и артерио-венозные мальформации. [87]. Следует отметить, что на тот момент каверномы считались крайне редкой патологией. К 1976 году в литературе описаны всего 164 случая, причем подавляющая их часть имела клинические проявления [128]. Значительные изменения в диагностике каверном (как и прочих заболеваний ЦНС) произошли после внедрения в клиническую практику КТ (1971 год), а затем и МРТ (1977 год). В конце 80-х годов прошлого века, на основании изучения патологии ствола головного мозга, Russell ввел термин «ангиографически скрытые сосудистые мальформации» («cryptic vascular malformation») [110], обозначающий сосудистые мальформации, не выявляемые при ангиографическом исследовании. К ангиографически скрытым сосудистым мальформациям были отнесены телеангиоэктазии, каверномы, венозные ангиомы, тромбированные АВМ и микро-АВМ. Семейная форма каверном впервые описана Kufs в 1928 году [70]. В течение длительного времени предполагалось существование генетического дефекта, связанного с формированием каверном. О возможном аутосомно-доминантном типе наследования сообщается в работах Bicknell и Hayman [20, 53]. Основополагающей по этой проблеме считается работа Hayman и соавт., 1982 г. [53]. В ней сообщалось о 122 родственных индивидуумах, обследованных с помощью КТ и АГ. У 5 больных были найдены ангиографически скрытые сосудистые мальформации, а у трех были обнаружены типичные каверномы. Среди 43 обследованных родственников у 15 также заподозрены каверномы. В работе был наглядно доказан аутосомно-доминантный путь наследования патологии с различной экспрессивностью. Далее были опубликованы данные исследований Rigamonti [106] и Mason [84], в которых было показано, что семейное наследование особенно велико среди испаноговорящих американцев. Детальные исследования случаев семейных каверном провели Zabramski и соавт. [138]. Авторы показали динамический характер заболевания, высокую вероятность изменения МР-характеристик каверном. На примере семейных форм достоверно показана возможность роста каверном и их de novo образования. Обследование группы испаноговорящих американцев с каверномами значительно помогло в выявлении генетической основы заболевания. Dubovksy [37] и Gil-Nagel [47] удалось локализовать ген, ответственный за проявление признака, расположенный в длинном плече 7-ой хромосомы. Guenl заподозрил и начал поиск фаундер-мутаций, а Laberge-le описал связанные с развитием заболевания мутации преждевременного прекращения синтеза белка в CCM1. [51, 73]. В последствии Craig и соавт. [31] установили наличие еще двух локусов, связанных с семейными формами каверном: CCM2 в коротком плече 7-ой хромосомы и CCM3 в длинном плече 3-й хромосомы. Согласно последним данным, предполагается наличие четвертого гена [77].
1.2 Общие сведения о кавернозных ангиомах
Каверномы являются вторым по частоте сосудистым пороком после венозных аномалий развития и составляют 10—15% от всех сосудистых мальформаций ЦНС [15]. Согласно данным аутопсий и МРТ-исследований, распространённость каверном составляет от 0,4 до 0,8% [15, 74, 97, 107]. Средний возраст манифестации заболевания – 3-е – 5-е десятилетие жизни. Заболеваемость детей характеризуется двумя пиками: в 0—2 года и 13—16 лет. [74, 96]. Распространенность каверном является равной среди мужчин и женщин. В некоторых исследованиях указано на повышенную заболеваемость симптоматическими каверномами среди женщин. Согласно имеющимся данным, до 50% каверном могут быть наследственными. Более 50% пациентов с семейной формой заболевания имеют множественные каверномы. Для спорадических форм данная цифра не превышает 20% [15, 92, 106, 138]. Каверномы могут располагаться в любом отделе головного и спинного мозга. До 80% всех выявляемых каверном обнаруживаются супратенториально [11, 35, 100, 50].
Кавернозные мальформации могут проявляться различными симптомами. К наиболее частым симптомам относят головную боль, эпилептические припадки, неврологический дефицит. Для супратенториальных каверном эпилептические приступы являются самым распространенным симптомом (23—79% случаев). Кавернозные мальформации, расположенные в базальных ядрах или таламусе, часто проявляются сенсомоторным дефицитом. Они могут также проявляться различными гиперкинезами, таламическими болями, гемианопсией, глазодвигательными нарушениями, гидроцефалией. Все перечисленные выше симптомы могут сочетаться либо не сочетаться с кровоизлияниями из каверномы. Как уже было отмечено, с момента широкого внедрения в практику МРТ, все больше каверном являются случайными находками, либо проявляются лишь головными болями или другими неспецифическими симптомами.
1.3 Каверномы и эпилептические припадки
Эпилептические припадки – наиболее частый симптом при каверномах полушарий большого мозга. Согласно многочисленным исследованиям, каверномы являются одними из самых эпилептогенных внутримозговых патологических образований. Robinson et al. (1991) сравнили эпилептогенность супратенториальных каверном, артерио-венозных мальформаций и глиальных опухолей. По данным этого исследования, при идентичности локализации и размера образований с эпилептическими припадками были сочетаны 50—70% каверном, 20—40% артерио-венозных мальформаций и 10—30% глиальных опухолей [107]. Сама кавернома, в которой отсутствует нервная ткань, не является источником припадка. Считается, что припадки при супратенториальных каверномах индуцированы повторными микрокровоизлияниями из каверном, следствием которых являются такие эпилептогенные процессы, как глиоз и воспаление окружающего мозгового вещества. Процессы деградации компонентов крови происходят также в кавернах мальформации [35, 69, 83, 105]. В электронно-микроскопических исследованиях показана неполноценность эндотелиального слоя и базальной мембраны полостей каверномы, что сопровождается выходом содержимого каверн в окружающую мозговую ткань [26, 115]. В опытах на животных показана высокая эпилептогенность ионов железа и тяжелых металлов при их аппликации на кору головного мозга [69, 93, 94, 134]. В окружающем каверному мозговом веществе, по сравнению с нормальной мозговой тканью, выявляются повышенные уровни глицина и серина, что характерно для эпилептогенной ткани [129]. Согласно теории вторичного эпилептогенеза, длительно существующие эпилептогенные очаги способны приводить к образованию вторичных очагов на расстоянии от первичного патологического процесса [95]. Особенно легко вторичные эпилептогенные очаги образуются при локализации патологических образований в височной доле [75, 41]. Вероятность образования вторичных эпилептических очагов пропорциональна длительности существования эпилепсии и количеству припадков. Таким образом, закономерно предположение, что длительность заболевания может снижать противоэпилептическую эффективность простой каверномэктомии [28]. Ferrier и соавт. исследовали характер патологической активности у больных с мальформациями развития мозговой ткани и кавернозными мальформациями [42]. В работе показано, что наличие различных форм эпилептической активности чаще наблюдается у больных с длительным анамнезом эпилепсии и связано с худшим прогнозом по отношению к лечению эпилепсии.
В ряде работ проводилась оценка риска возникновения припадков. В ретроспективном анализе Kondziolka [67] эпилептический синдром развился у 4.3% пациентов после постановки диагноза. Согласно данным ретроспективной работы Del Curling [46], риск припадка для бессимптомных каверном составляет 1.5% на человека в год. По данным Moriarity [92] риск развития эпилептического синдрома вследствие наличия каверномы у больных без припадков составляет 2.4% на пациента в год. Кортикальное расположение каверномы считается безусловным фактором риска развития эпилепсии. В некоторых исследованиях повышенный риск развития эпилептического синдрома связывают с локализацией каверном в медиальных отделах височной доли, множественными каверномами, размером кольца перифокальных изменений мозга и мужским полом [89, 12, 35, 24, 90]. Согласно мнению некоторых авторов, каверномы, расположенные в сенсомоторной коре, являются более эпилептогенными [30]. По данным обзора Moran и соавт, обобщающего данные по 296 пациентам, оперированным по поводу супратенториальных каверном, статистически значимая связь между локализацией и вероятностью развития эпилептических припадков отсутствует (таблица 1).
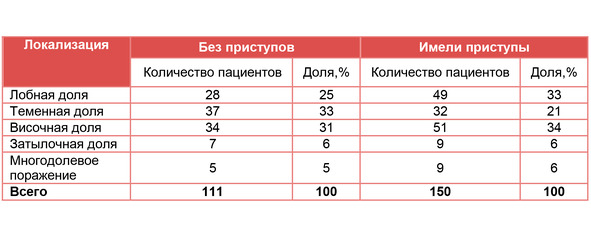
Таблица 1. Наличие эпилептических приступов у больных с каверномами определенных локализаций по данным Moran и соавт. [90].
Структура эпилептического синдрома у одного пациента может быть стабильной на протяжении всего заболевания, либо меняться с течением времени за счет учащения приступов и изменения их характера. В большей части работ анализ приступов произведен на основании классификации по ILAE 1983 года (см. далее), с выделением простых парциальных, сложных парциальных, первично и вторично генерализованных приступов. В большинстве случаев при эпилепсии, обусловленной наличием объемного образования супратенториальной локализации, наблюдаются фокальные (простые или сложные) или вторично-генерализованные приступы [4]. Эпилептические припадки, связанные с супратенториальными каверномами, в 27—63% случаев являются генерализованными, в 6—45% случаев – сложными и в 27—31% случаев исключительно простыми фокальными [78, 112, 132, 90]. Частота припадков варьирует в очень широких пределах – от одного припадка в несколько лет до нескольких приступов в день. У многих больных отмечается четкая тенденция к учащению приступов на протяжении развития болезни (может наблюдаться и на фоне противосудорожной терапии). Замечено, что значительная доля генерализованных припадков связана с патологией лобной доли. Каверномы височной доли в значительно меньшем количестве случаев проявляются генерализованными припадками, чем при любой другой локализации [90].
1.4 Каверномы и кровоизлияния
Возможность кровоизлияния является одним из основных фактов, склоняющих к рассмотрению необходимости хирургического лечения. Безусловно, выраженность кровоизлияния редко бывает столь драматической, как при разрыве артериальных аневризм или АВМ, однако и при кровоизлияниях из каверном возможна грубая инвалидизация или летальный исход.
Кровоизлияния являются общепризнанной причиной развития любой неврологической симптоматики при каверномах ЦНС. Данный факт подтверждается тем, что в окружающем мозговом веществе всегда находят признаки кровоизлияний различной давности. Рентгенологическая и/или ликворологическая верификация геморрагических событий возможна только в случае «классического» кровоизлияния, однако, массивные кровоизлияния с развитием типичной клинической картины случаются значительно реже, чем повторные микрогеморрагии [35, 107]. Понятие кровоизлияния значительно различается от исследования к исследованию, что создает сложности в оценке риска кровоизлияния. В некоторых работах кровоизлиянием из каверномы объясняются любые изменения состояния пациента. Другие исследователи полагаются исключительно на результаты нейровизуализации. Таким образом, существует большой разброс в данных о частоте кровоизлияний при каверномах: от 9% до 88%. Ввиду диагностических сложностей, как очевидные геморрагии, так и любое острое развитие неврологической симптоматики предложено называть «неврологическим событием» [100]. Повторными кровоизлияниями различного характера можно объяснить как пароксизмальность течения болезни, так и своеобразие течения эпилептического синдрома. Следует также отметить, что в большой части исследований годовой риск кровоизлияния вычисляется исходя из представлений о врожденном характере патологии. С учетом имеющихся данных о возможности образования каверном de novo, ретроспективный анализ может давать недостаточно точный результат.
Одними из первых оценку риска кровоизлияния выполнили Del Curling и соавт. [35]. В их исследовании проведена ретроспективная оценка 8000 МР-томограмм и найдено 32 каверномы (0,39%). Риск симптоматического кровоизлияния определен цифрой 0.25% на пациента в год и 0.10% на каверному в год. В работе Robinson [107] ретроспективно оценены МР-изображения более 14 000 пациентов, выявлены 66 пациентов с 76 каверномами. Частота встречаемости каверном составила 0.47%. Частота клинически значимых кровоизлияний составила 0.7% на каверному в год. В работе Kim [63] ретроспективно проанализированы данные по 62 больным с 108 каверномами. Большее число каверном проявились клинически, 12% каверном были бессимптомны. Риск клинически значимого кровоизлияния составил 2.3% на пациента в год, 1.4% на каверному в год. Отдельного внимания заслуживают данные, полученные Zabramski и соавт. [138]. Исследователи провели большую работу по изучению естественного течения болезни у больных с семейной формой каверном ЦНС. Риск клинически значимого кровоизлияния составил 6.5% на пациента в год и 1.1% на каверному в год. В данном исследовании также проведена оценка частоты бессимптомных кровоизлияний, которая составила 13% на пациента в год и 2% на каверному в год.
За последние годы было опубликован ряд других исследований естественного течения заболевания, большинство из которых указывают на вероятность кровоизлияния для суб- и супратенториальных каверном в диапазоне от 0,7 до 6% на пациента в год (0,1% до 2,7% на каверному в год и от 0,013% до 16,5% на пациента в год, согласно последнему крупному обзору Washington и соавт. [131], таблица 2).
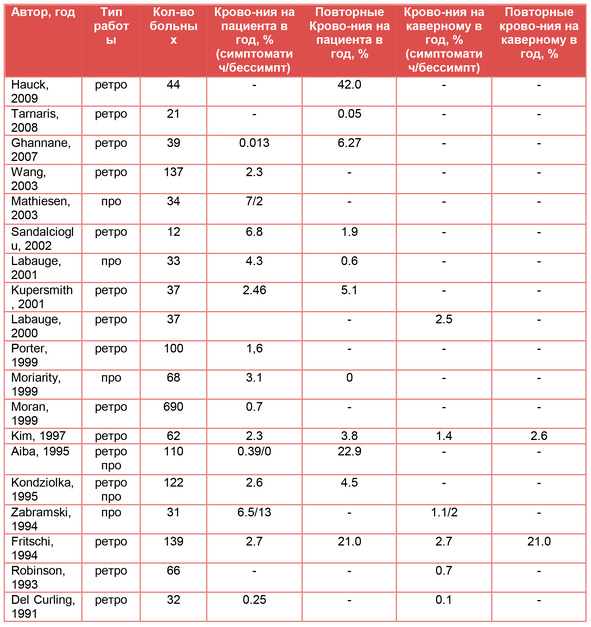
Таблица 2. Риски кровоизлияния из каверном по данным различных исследований (по Washington и соавт., [131])
Одним из широко известных факторов, увеличивающих вероятность кровоизлияния, является предшествующее кровоизлияние в анамнезе. Согласно различным работам, вероятность повторного кровоизлияния превышает риск первичного в 2—10 раз. Одним из первых крупных исследований, посвященных этому вопросу, является работа Aiba и соавт. [10]. В этом ретроспективном исследовании на материале 110 больных с каверномами выявлены значительные различия между рисками первичного и повторного кровоизлияния: 0,39% против 22,9%. В других исследованиях показаны схожие результаты. Kondziolka и соавт. [67] выполнили ретроспективно-проспективное исследование на материале 122 больных, находящихся под наблюдением и получающих консервативное лечение. В работе установлено, что частота клинически значимых кровоизлияний для пациентов без кровоизлияний в анамнезе составляет 0,6% на пациента в год, а для больных, перенесших кровоизлияние – 4,5% на пациента в год. В исследовании Moriarity и соавт. [92] проспективно наблюдались 68 пациентов с 228 каверномами. Общий риск кровоизлияния на пациента в год составил 3.1%. Хотя они не подтвердили того, что кровоизлияние в анамнезе является самостоятельным фактором риска рецидива, они установили, что пациенты с очаговым неврологическим дефицитом, связанным или не связанным с кровоизлиянием, имеют больший риск кровоизлияния из каверномы (8,9% против 0,4% на пациента в год).