
Хлопок одной ладонью
Кислород и углерод как элементы воплощают в себе свойства, которые после возникновения жизни лягут в основу метаболизма, или обмена веществ. Метаболизм имеет две стороны. Анаболизм – строительство больших молекул с затратой энергии, то есть почти всегда строительство углеродных цепочек. Катаболизм – расщепление больших молекул с выделением энергии, то есть, в современной природе, почти всегда сжигание углеродной пищи кислородом. Вместе анаболизм и катаболизм замыкаются в энергетический цикл, способный приспосабливаться к любым нуждам живого организма, и в этом цикле заключается одно из самых главных, самых чудесных свойств жизни. Любой живой организм имеет сложную систему «обмена валюты», которая связывает анаболизм с катаболизмом. Эта восхитительная система позволяет нам запихивать в рот почти все что угодно и каким-то образом безо всяких усилий превращать спрятанную там химическую энергию в мысли и движения.
Можно сказать, что метаболизм – это половина того, что значит быть живым. Но цикл энергии, в принципе подходящий под определение обмена веществ, встречается во многих системах (например, любой природный круговорот). В понятие живого организма, по крайней мере в известных нам земных вариантах, входит, помимо метаболизма, еще один цикл: информационный. Живые организмы обладают наследственностью. Но, перед тем как я произнесу слово на букву «г», предлагаю отвлечься на легкий пересмотр природы реальности.
Мир как рецепт пирожкаВ бытовом смысле мы используем слово «информация» для обозначения значимого и обычно передаваемого знания. Информация передается, когда два человека разговаривают. При чтении информация преобразуется из письменной формы в мысленную. Информация копируется, если переслать файл с одного компьютера на другой. Может показаться, что само понятие информации возникает в тот момент, когда что-то значимое куда-то передается. То есть с бытовой точки зрения информация – это «мера общения», слово, обозначающее передачу каких-то важных параметров из одной системы в другую.
С более формальной, физической точки зрения информация совсем необязательно должна куда-то копироваться или что-то значить, чтобы быть информацией. Информация – это не передача параметров, это сами параметры. Абстрактное описание системы, отличающее ее от других систем. Например, в доме содержится информация о взаимном расположении кирпичей, и эта информация существует независимо от самих кирпичей, от вашего знания об этих кирпичах и вообще от материального мира. Она может быть нигде не записана и никому не известна, но она то, что отличает дом от груды кирпичей. Информация – не столько «мера общения», сколько «мера порядка», индекс свойств системы, выделяющий ее из хаоса. Она «содержится» в материи, но существует независимо. Например, роман «Война и мир» – это информация, абстрактное описание того, как должны быть расположены буквы на листе, чтобы отражать задумку автора. Эта информация может содержаться в бумажной книге или в памяти компьютера, но эти материальные носители – не то же самое, что великий роман русского классика.
С этой точки зрения можно еще раз взглянуть на Вселенную в целом. Из чего она состоит? Допустим, что всю Вселенную взяли, стерли в порошок и распылили до гомогенного пара. Суммарное количество энергии останется точно таким же, даже количество атомов и частиц вряд ли изменится (зависит от того, как стирать в порошок). Что исчезнет при таком стирании – так это информация. Распределение атомов и энергии между реками и морями, материками, планетами и галактиками, распределение, благодаря которому они были собой. Не будет ли логичным сказать, что из информации Вселенная и состоит? Энергия – это начинка Вселенной, а информация – рецепт вселенского пирожка. Вот вам и легкий пересмотр реальности.
Что делает жизнь живой? Способность воспроизводить информацию. Точнее, способность информации воспроизводить саму себя. Но все по порядку.

Молекула всего
Принципиальны для понимания жизни два типа молекул: белки и нуклеиновые кислоты.
Это огромные молекулы, если смотреть на них с точки зрения неживой природы. Допустим, вы атом углерода – как мы помним, четверорукий крепкий хозяйственник, из которого в основном выстроены молекулы живого организма.
Допустим, ваш диаметр соответствует человеческому росту. В таких координатах средний белок будет размером эдак со Спасскую башню или статую Свободы, а рибосома – машина для изготовления белков – примерно с футбольный стадион. Матричная РНК – программа, которая в эту машину вставляется, – окажется лентой шириной в 20 метров, а длиной в десятки километров. ДНК – две похожие ленты, закрученные друг вокруг друга, но ленты настолько длинные, что это, скорее, дороги, ведущие из ниоткуда в никуда. У бактерий ДНК замкнута в огромное кольцо окружностью в половину, а иногда и весь земной экватор. У человека ДНК не кольцевая, поэтому начало и конец у нее все-таки есть, зато длина человеческой ДНК во много раз больше бактериальной. В наших воображаемых координатах расстояние между двумя концами ДНК в человеческой хромосоме – порядка расстояния от Земли до Луны. Оно и в обычных, реальных-то координатах впечатляет. Каждая хромосома – это одна молекула ДНК, намотанная на плотно упакованные катушки из белков-гистонов, а всего хромосом в каждой клетке 46 штук. Если хромосомы размотать, то в каждой клетке человека обнаружится аж два метра ДНК3.
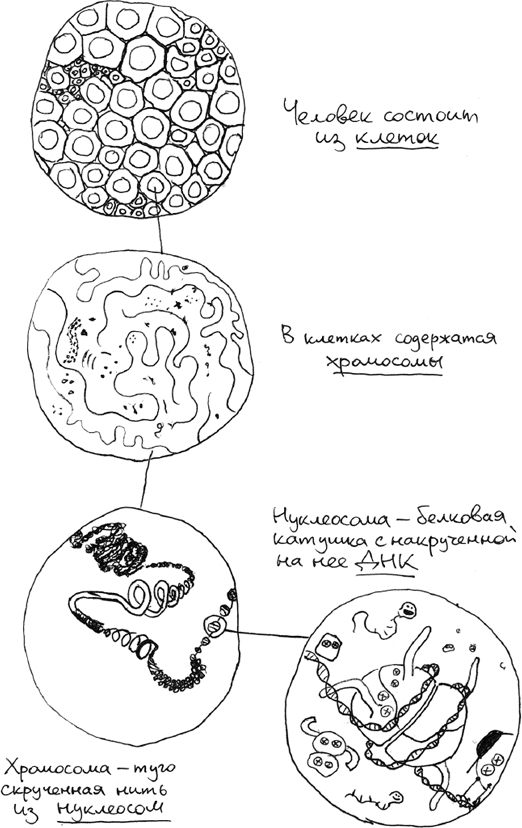
Белки – совершенно несуразное название для чего-то настолько важного и величественного. Что такое белок, знает каждый ребенок: белок – это белая, по-моему, менее вкусная часть яйца. Какая связь между яичным белком, прозрачным желе, белеющим при нагревании, и белками, из которых состоит наше тело, понять очень сложно. Яичная аналогия помогает усвоить, что белки очень питательные, но мешает понять, что белок вовсе не гомогенная масса одного и того же вещества.
Ту же, в общем, идею однородности белкового вещества выражает синоним «белка» – «протеин». Предложил его в 1838 г. шведский ученый Йёнс Якоб Берцелиус в письме голландскому химику по имени Геррит Ян Мульдер4. Мульдер изучал химический состав разных биологических субстанций (шелка, яиц, плазмы крови) и пришел к убеждению, что в основе всего живого лежит одна и та же сущность, «первовещество». Мульдер фантазировал, что это первовещество производить умеют только растения и в этом заключается их питательная ценность для животных. Берцелиус – выдающийся шведский химик, с которым Мульдер много лет переписывался, – предложил так это первовещество и назвать: протеин, от слова πρώτειος, то есть «первичный» по-гречески.
Все оказалось несколько иначе, чем предполагал Мульдер. «Первовещества» как такового на самом деле нет. Все сложные молекулы, из которых мы состоим, производят наши собственные клетки из простейших деталей, причем организм великолепно умеет изготавливать одни детали из других. Некоторые детали должны обязательно поступать с пищей, как, например, половина аминокислот – из них состоят белки. Но в целом живой организм обходится тем, что имеет. Как правило, он может сожрать что угодно, разобрать практически на атомы и собрать в любые нужные ему молекулы. Поэтому идея о том, что растения производят некий единый белок, из которого состоят животные, неверна. Тем не менее Мульдер действительно нащупал кое-что важное и общее между изучаемыми им субстанциями. Просто они оказались не одним и тем же белком, а разными белками. Белок – не одна какая-то молекула, а тип сложного химического соединения, представляющий собой разнообразные цепи из одинакового набора деталей, бусин, аминокислот. То есть химически белки очень похожи друг на друга, что и натолкнуло химика Мульдера на мысль о «первовеществе». Но главное в белке то, что разные последовательности бусин позволяют создавать совершенно разные молекулы из одного и того же набора компонентов.
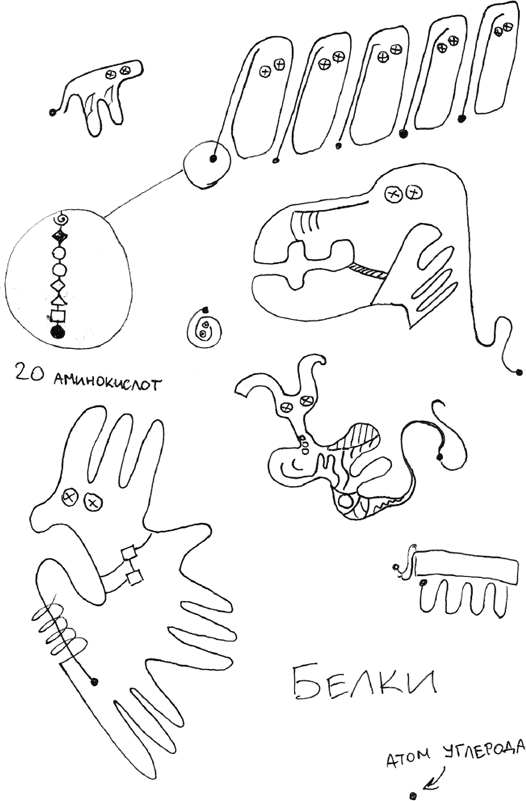
Эти разнообразные белки правят живым организмом. Как рабочие разных профессий, они делают все, что только можно в нем делать. Мы перевариваем пищу с помощью белков, дышим кислородом с помощью белков, двигаемся с помощью белков. Белки копируют ДНК, синтезируют клеточную мембрану, а при формировании долгосрочной памяти белки в гиппокампе отправляют при помощи белков белковые сигналы другим белкам в кору. Всего у человека порядка 20 000 разных белков5, но каждая клетка решает, когда и в каких количествах производить из них тот или иной белок.
В общем, как «первовещество» термин «протеин» себя не оправдал: белок – это не одна вещь, а огромное количество похожих вещей. Я предлагаю простое решение вопроса: можно переосмыслить этимологию слова как отсылку к греческому богу Протею, морскому божеству, способному принимать разные формы. Тогда все встает на свои места. Так или иначе, «протеин» – слово, конечно, поэлегантнее, чем «белок», но, к сожалению, в русском языке так белки называют только продавцы биодобавок. Так что придется терпеть яичную терминологию. Белки так белки.
Нуклеиновые кислоты – название еще хуже. Во-первых, длинное, сложное, учебником химии веет за километр. Во-вторых, тот факт, что нуклеиновые кислоты именно кислоты, конечно, многое определяет в их химических свойствах, но для общего понимания их смысла совершенно не принципиален. Да и «нуклеиновость» этих кислот, в общем, вторична. Nucleus означает «ядро», отдел клетки, в котором у нас, эукариот, нуклеиновые кислоты хранятся. У бактерий – самой многочисленной формы жизни на Земле – ядер нет, а кислоты все равно нуклеиновые.
Что такого важного в нуклеиновых кислотах – ДНК и РНК? Сами по себе, то есть без белков, они почти беспомощны. За редкими (хотя и важными) исключениями, о которых речь впереди, нуклеиновая кислота тихо лежит, а белки с ней что-то делают. Сила нуклеиновых кислот не в работоспособности или многофункциональности, а в том, что они несут информацию о том, какими нужно быть белкам, чтобы исполнять нужные функции. Нуклеиновые кислоты кодируют белки. Белки на самом деле – это не рабочие, а роботы. Они изготавливаются по специальным программам, записанным в нуклеиновых кислотах.
Физически и белки, и нуклеиновые кислоты представляют собой цепи, сложенные из последовательностей повторяющихся деталей, блоков, бусин. Белки состоят из блоков, называемых аминокислотами, нуклеиновые кислоты – из блоков, называемых нуклеотидами.
В белках 20 возможных составных частей, причем все они очень разные с химической точки зрения. Аминокислоты – это как набор «Юный химик». Все их можно комбинировать в почти бесконечном количестве вариантов. Благодаря разным последовательностям аминокислот разные белки приобретают разные свойства, изгибаются в сложные трехмерные формы, покрытые всевозможными химическими группами, работающими как детали машины. Это обилие компонентов и комбинаций дает белкам такое бесконечное разнообразие функций. В конечном итоге все сводится к простейшему рецепту: такие-то аминокислоты в такой-то последовательности. Информация определяет функцию. Последовательность белка решает, что этот белок умеет делать.
Четырехбуквенный романЧто касается нуклеиновых кислот, то они бывают двух типов: рибонуклеиновая (РНК) и дезоксирибонуклеиновая (ДНК). По молекулярному составу они очень похожи друг на друга, но их роли и значение совершенно разные. О РНК разговор впереди, пока же для простоты можно ограничить нуклеиновые кислоты знаменитой двойной спиралью ДНК.
В ДНК всего четыре составные части, причем не так сильно различающиеся по химической сущности. Но эти составные части, нуклеотиды, обладают ключевым свойством, носящим название комплементарности. Комплементарность – это способность одной цепи нуклеотидов связываться с другой комплементарной цепью нуклеотидов, если их последовательности соотносятся как негатив и позитив. Иначе говоря, это способность одной цепи задавать другую цепь, и наоборот.
Благодаря этому свойству нуклеотидные цепи идеально подходят для воспроизведения особого типа информации, которую называют наследственной информацией, генетической информацией или просто генами. (Вот оно, слово на букву Г!) Все гены организма в совокупности называются геномом[1]. Ген – это фрагмент генома, как глава – фрагмент романа. Геном записан в ДНК, как роман записан в книге.
Каждая цепь ДНК состоит из четырех возможных нуклеотидов: аденин, гуанин, цитозин и тимин. Их иногда даже называют для простоты «буквами»: А, Г, Ц и Т. Эти буквы связаны друг с другом последовательно, как бусины: например, Т-Ц-Ц-Г-А. Благодаря химической структуре четырех нуклеотидов, такая цепь может связаться с другой, параллельной цепью, причем к А подходит только Т, а к Г – только Ц, и наоборот. То есть парная цепь в нашем примере: А-Г-Г-Ц-Т. Две эти цепи, встретившись, обовьются друг вокруг друга и образуют двойную спираль, а две другие цепи со случайными, не подходящими друг к другу последовательностями ее не образуют. Такую «парность» двух цепей и называют комплементарностью, а сами парные последовательности – комплементарными.
Чем так принципиальна комплементарность? Благодаря тому, что последовательность одной цепи «знает» последовательность другой цепи, ДНК можно копировать. Имея две цепи, достаточно знать последовательность одной из цепей, чтобы восстановить всю исходную молекулу. Это происходит при делении любой клетки. ДНК разматывается из двойной спирали на две отдельные нити, и недостающая нить достраивается специальными белковыми роботами по принципу комплементарности. В итоге образуются две одинаковые двойные спирали, которые распределяются между дочерними клетками3.
То есть нуклеиновые кислоты, благодаря своей химической структуре, позволяют копировать содержащуюся в их последовательности информацию. В каком-то смысле комплементарные цепи ДНК – это воплощение самой идеи жизни. Удвоение, копирование, размножение, деление – все это синонимы, когда речь идет о ДНК. (Вдумайтесь: только в биологии множить и делить – это одно и то же.) Даже производство Евы из ребра Адама следует тому же самому принципу, что и копирование последовательности ДНК: имея часть исходника, восстанови недостающее.
Но самое главное в том, что эта самая генетическая информация, последовательность нуклеотидов, так хорошо приспособленная к копированию, имеет скрытый смысл, который в ней можно прочесть, если знать шифр. Последовательность нуклеотидов – не просто молекулярные бусы. Это код. Информация в ДНК означает последовательность белка, а вместе с ней – то, что белок делает: дыхание, движение, питание, и все остальные функции живого организма. С помощью этого своего кодирующего свойства бездейственная ДНК, тихо хранящая в себе мудрость поколений, манипулирует окружающим миром, извлекая из себя информацию о полчищах белковых роботов.
Роботы кодируются четырехбуквенным кодом, в котором каждой аминокислоте соответствует «слово» из трех букв: АТТ – изолейцин, ГЦЦ – цистеин и так далее. Всего возможны 64 таких слова, и они распределены между 20 аминокислотами и специальными обозначениями «конец белка»: ТАА, ТАГ и ТГА. Если часть последовательности ДНК прочитать со специальным словарем, то получится последовательность белка.
КСТАТИ
Словарь перевода с нуклеотидного на аминокислотный называется генетическим кодом. Генетический код – это не то же самое, что генетическая информация. Генетическая информация – это все, что записано в ДНК. Генетический код – это таблица из 64 трехбуквенных комбинаций нуклеотидов, или кодонов, и соответствующих аминокислот, которые они кодируют. «Таблица кодонов» висит над столом у многих биологов наподобие таблицы Менделеева у химиков или, наверное, карты метро у работников метрополитена – требуется часто, теоретически можно и запомнить, но зачем?
В живой клетке есть специальная машина, ответственная за «перевод со словарем». Этот огромный молекулярный комплекс под названием рибосома – точка, в которой производятся белки и в которой нуклеиновые кислоты сообщают им свою генетическую волю. Здесь принципиальной становится вторая из кислот, рибонуклеиновая, она же РНК, родственница вездесущей двойной спирали. Пора составить семейный портрет.
В центре догмыДНК строга, спокойна, склонна к стабильности. Ее роль – нести свое знание из поколения в поколение с максимальной точностью. Она как жрица, живущая под грузом вечности: в ней содержатся гены, исчисляющие время эпохами. ДНК – это обычно гигантская цепь из миллионов нуклеотидов, и разные белки записаны в разных участках этой цепи. Гéном, в принципе, можно называть любой участок ДНК. По Ричарду Докинзу, например, ген – «единица, продолжающая существовать в ряду многочисленных последовательных индивидуальных тел»6. Но обычно в качестве такой единицы выбирают участок ДНК, обозначающий один белок.
РНК куда менее стабильна, чем ДНК, – постоянная головная боль для биохимиков, пытающихся ее исследовать. Она ретива и мимолетна, но в каком-то смысле гораздо более талантлива, чем ее статная родственница ДНК. ДНК не умеет делать ничего и только торжественно хранит покой содержащихся в ней генов. РНК не сравнится с белком в плане талантов, но в принципе умеет делать множество вещей, иногда даже вступая в принципиально важные химические реакции. Ее жизнь коротка, а по размерам она редко превышает тысячу-другую нуклеотидов (хотя и при такой длине РНК крупнее большинства белков).
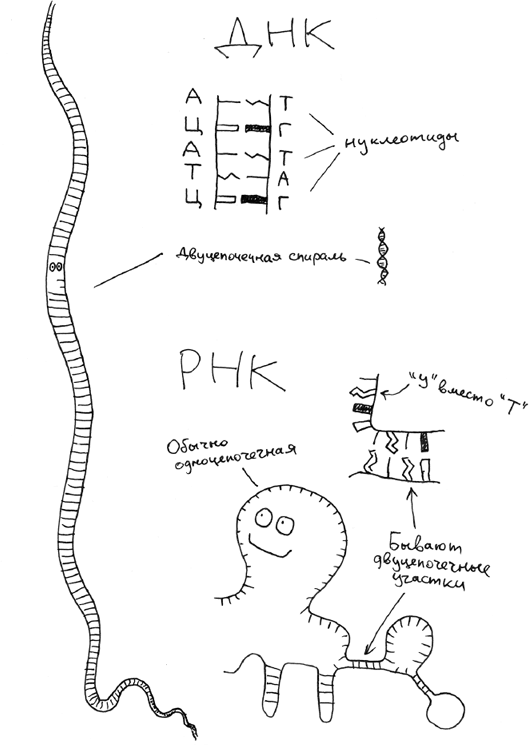
РНК – это копия одного из участков ДНК. Она как бы распечатка одного из тысяч негативов, хранящихся в архиве. Сделать такую распечатку можно, конечно, благодаря комплементарности. На одну из цепей ДНК садится специальный белок, называемый РНК-полимеразой, и собирает комплементарную ей цепь, только состоящую из слегка отличающихся нуклеотидов. В реальном времени РНК-полимераза скорее летит вдоль цепи ДНК, а растущая копия – цепь РНК – змеится за ней хвостом. Весь процесс «распечатки» называется транскрипцией. Транскрипция – это изготовление РНК на базе последовательности ДНК.
КСТАТИ
Нуклеотиды в РНК называются рибонуклеотидами, а в ДНК – дезоксирибонуклеотидами, в последних на один кислород меньше, отсюда «дезокси». Помимо этого отличия, есть еще одно: в РНК вместо тимина (Т) используется урацил (У). Ничего важного для понимания при этом не меняется. Это примерно как отличие украинского алфавита от русского – не очень значительные, исторически сложившиеся различия в буквах.
Цепь РНК как таковая по химической структуре почти идентична ДНК, но из-за небольших отличий в нуклеотидах ведет себя иначе. РНК не склонна к длинным цепям и двойным спиралям, хотя это и возможно: двухцепочечная РНК есть, например, у некоторых вирусов. Вместо двойных спиралей, в которых друг к другу прилипают целые комплементарные цепи, одиночная цепь РНК живет сама по себе, но любит изгибаться в сложные трехмерные структуры – совсем как белок. Это происходит за счет комплементарного «слипания» разных участков одной и той же цепи РНК, изгибающего молекулу в том или ином направлении. В совокупности с большей, чем у ДНК, реакционной способностью все это ставит РНК в каком-то смысле посередине между двумя главными молекулами природы. По своей сущности РНК – почти ДНК. Она состоит из нуклеотидов и может транскрибироваться («распечатываться») с одной из цепей двойной спирали. Но по своей склонности к сложным трехмерным формам и готовности вступать в химические реакции РНК – почти белок.
С транскрипции начинается путь гена – информации, записанной в ДНК, – в материальный мир. Поэтому одна из основных задач клетки состоит в регуляции транскрипции. Клетка населена армиями белков, называемых транскрипционными факторами, которые занимаются исключительно тем, что включают и выключают транскрипцию тех или иных участков ДНК в зависимости от всевозможных сигналов, получаемых ими от других белков или из окружающей среды. Говоря, что клетка «включает» какой-нибудь ген, биологи в большинстве случаев имеют в виду включение транскрипции этого гена.
Ген, скопированный в свежую цепочку РНК, внезапно обретает мобильную форму. В таком виде он может путешествовать по клетке и даже между клетками, взаимодействовать с белками, а иногда складываться в «белковоподобные» трехмерные машины. Но особым статусом пользуются РНК, которые сами ни во что сложное не складываются и ничего интересного не делают, а только смиренно несут в себе генетическое послание, на основе которого будет изготовлен белок. В английском языке их так и называют: messenger RNAs, «РНК-посланники». В русском языке аббревиатура мРНК обычно расшифровывается как «матричные», что отражает их суть (эти РНК служат матрицей для изготовления белков), но немного лишает душевности[2].
Куда несут свое послание РНК-посланники? На рибосому. Это, напомню, огромная молекулярная машина, можно сказать станция, на которой производятся белки, где нуклеотидный язык переводится на аминокислотный. Она умеет брать «генетическое послание», матричную РНК, и, пропуская через себя шагами в три нуклеотида, параллельно собирать соответствующий белок, бусина за бусиной. В зависимости от того, какую матричную РНК вставить в рибосому, она может произвести любой белок. Рибосому можно считать древнейшим компьютером, работающим по алгоритму генетического кода.
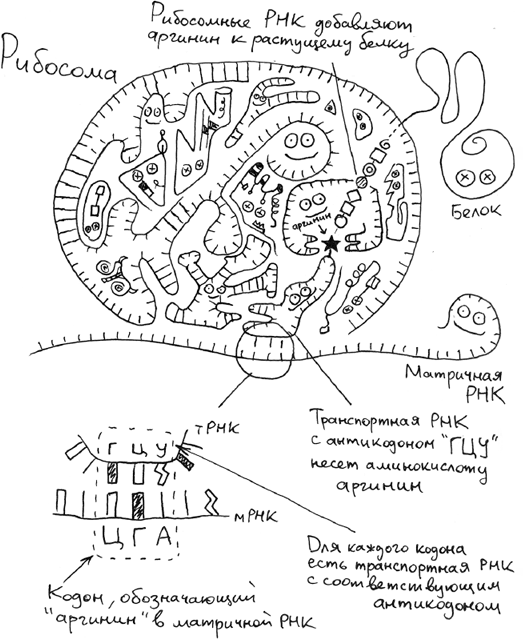
РНК-полимераза (белок, который «распечатывает» гены в РНК) и рибосома (машина, которая «переводит» РНК в белок) в совокупности делают принципиально важную вещь: они придают информации форму. Ген – абстрактная идея, записанная в последовательности нуклеотидов, – никак не влияет на мир до тех пор, пока не обретет физическое тело, отдельное от бесконечного рулона ДНК. Транскрипция дает ему материальную жизнь в форме РНК; трансляция в белок дает ему способность управлять внешним миром. Именно свойствами белков определяются свойства живого организма. Белки решают, как работает пищеварение. Белки решают, какой формы нос. Белки решают, с какой скоростью двигается по мозгу нервный импульс.
Этот процесс превращения информации в функцию в биологии называется Центральной догмой. Центральная догма – что-то вроде биологического закона, универсальный принцип работы любого известного нам живого организма. Земля вертится вокруг Солнца, дважды два – четыре, белок считывается с гена, а ген с белка – нет.
КСТАТИ
Обычно Центральную догму рисуют в «тройном» виде: ДНК→РНК→белок. Имеется в виду, что в живых организмах информация всегда движется в этом направлении, а в обратном направлении не движется. Сформулированная таким образом в 1960-е гг. Центральная догма, впрочем, быстро пошатнулась, когда были открыты ретровирусы. Те умеют изготавливать ДНК на базе РНК. Так поступает, например, вирус иммунодефицита человека. Его геном записан в форме РНК, но при попадании в человеческую клетку он изготавливает свою ДНК-версию и встраивается в геном хозяина. Процесс производства ДНК на матрице РНК называется обратной транскрипцией, а «ретро-» в названии ретровирусов по той же причине означает «назад». То есть ретровирусы – вирусы-оборотни.
В дальнейшем нашлись и другие примеры синтеза ДНК из РНК, поэтому репутация Центральной догмы как аксиомы была подпорчена. И все же если схему перерисовать в «двойном» виде, то ее действительно можно считать неколебимым законом живого: нуклеиновые кислоты→белки.
Или еще абстрактнее: информация→функция.
Последний универсальныйЗадача этой книги – представить себе историю живого в виде последовательности реальных событий, мгновений прошлого, ключевых точек во времени, определивших нашу сегодняшнюю жизнь как разумных существ. Первым и главным из таких событий должен стать, несомненно, момент возникновения жизни на Земле. Проблема в том, что мы решительно ничего о нем не знаем. Не знаем, что произошло, не знаем – где, не знаем – когда, не знаем даже, что именно происхождением жизни нужно считать.
Например, мы не знаем, было ли возникновение жизни единичным событием. Вполне вероятно, что жизнь зарождалась многократно даже на нашей планете, не говоря уже о других потенциально возможных мирах. Но сколько бы раз это ни происходило, можно с достаточной долей уверенности утверждать, что вся ныне существующая жизнь на Земле берет свое начало от одного-единственного предка. Свидетельствует об этом простой факт: вся современная жизнь, от бифидобактерий до носорогов, работает по одному и тому же принципу: информация хранится в ДНК и выражается (по-биологически – экспрессируется) в белках при посредничестве РНК.