
Внутренние болезни
Следует соблюдать осторожность при применении этих препаратов у больных, предварительно длительно получавших β-адреноблокаторы и диуретики, из-за возможности резкого снижения артериального давления. Не рекомендуется назначать их для коррекции артериальной гипертензии при беременности. Противопоказанием к назначению ингибиторов является двусторонний стеноз почечных артерий или стеноз артерии единственной почки. Частота побочных эффектов при применении ингибиторов определяется дозой препарата, длительностью его применения и состоянием экскреторной функции почек. К числу наиболее часто встречающихся побочных действий относятся сыпи и кожный зуд (до 14 %), нарушение вкуса (около 5 %), нарушения со стороны желудочно-кишечного тракта (до 5 %) и кашель (от 1 до 15 %). Наиболее серьезными осложнениями являются почечная недостаточность, нефротический синдром и гипоплазия кроветворения.
Блокаторы первого типа рецепторов к ангиотензину-II (АТ1-блокаторы). В настоящее время применяются 3 препарата: лосартан (25 – 150 мг/сут.), валсартан (80 – 160 мг/сут.) и ирбесартан (150 – 300 мг/сут.).
Механизм действия АТ1-блокаторов обусловлен блокадой первого типа рецепторов к ангиотензину-II, что приводит к снижению артериального давления, обратному развитию гипертрофии миокарда и изменениям сосудистой стенки. Кроме того, при блокаде первого типа рецепторов усиливается влияние второго типа рецепторов ангиотензина-II, действие которых на ткани в значительной мере противоположно влиянию рецепторов первого типа. Эти препараты отличает хорошая переносимость. Влияние АТ1-блокаторов на сердечно-сосудистую систему существенно не отличается от такового ингибиторов ангиотензинпревращающего фермента.
Блокаторы медленных кальциевых каналов (кальциевые антагонисты). В терапии больных ГБ используются три группы кальциевых антагонистов (табл. 1.5). Они уменьшают поступление кальция в гладкомышечные клетки сосудов и кардимиоциты через потенциалзависимые L-кальциевые каналы и используются в качестве как единственного препарата, так и при комбинированной терапии.
Таблица 1.5
Доза и частота приема наиболее широко используемых в клинике кальциевых антагонистов

Верапамил и дилтиазем наиболее показаны пациентам с исходной тахикардией. Противопоказаниями к назначению являются сердечная недостаточность, синусовая брадикардия, нарушения синоаурикулярной и атриовентрикулярной проводимости.
Дигидропиридинам следует отдавать предпочтение при исходно нормальном числе сокращений сердца или брадикардии. Они не рекомендуются к применению при сопутствующем аортальном стенозе или сердечной недостаточности. Большинство побочных эффектов, отмечаемых при приеме дигидропиридинов, обусловлено вазодилатацией и рефлекторной активацией симпатической нервной системы. У ряда больных возникают отеки, наиболее часто локализованные в области голеней и стоп.
Прямые вазодилататоры. Из препаратов этой группы в клинике используются гидралазин (таблетки по 50 и 100 мг) и миноксидил (таблетки по 1 мг). Обычно их применяют в комбинации с другими препаратами при отсутствии желаемого снижения артериального давления. Начальная доза гидралазина – 10 мг 2 – 3 раза в сутки, миноксидила – 2 – 4 мг, средние терапевтические дозы – 100 мг и 20 мг соответственно. К числу наиболее частых побочных действий относятся сердцебиение, покраснение лица, головные боли, головокружения, ортостатическая гипотензия, возможны провокация аритмий и стенокардии, задержка натрия и воды.
Особенности медикаментозной терапии. При умеренном повышении артериального давления возможно назначение одного препарата. Четкие критерии выбора того или иного препарата отсутствуют. Он определяется «симпатиями» врача к определенной группе препаратов, доступностью препарата, его переносимостью, экономическими соображениями (стоимость препарата), выраженностью антигипертензивного действия у каждого конкретного больного. Тем не менее сегодня на основании анализа результатов многочисленных исследований могут быть даны определенные рекомендации по выбору препаратов.
Сегодня в большинстве стран при лечении больных гипертонической болезнью наиболее часто используются β— и α-адреноблокаторы, диуретики (гипотиазид, индапамид), ингибиторы ангиотензинпревращающего фермента, блокаторы АТ1-рецепторов и кальциевые антагонисты. Все они могут назначаться в качестве первого препарата. У пациентов без сопутствующей патологии терапию можно начинать с применения β-адреноблокаторов и/или диуретиков.
Для лечения пациентов этой группы в нашей стране наиболее часто используются β-адреноблокаторы. Кроме того, в качестве единственного гипотензивного средства могут быть рекомендованы кальциевые блокаторы, диуретики, ингибиторы конвертирующего энзима, α-адреноблокаторы, клофелин и моксонидин. Допегит, резерпин и вазодилататоры используются лишь у единичных пациентов.
Наиболее четкий эффект оказывают β-адреноблокаторы у лиц молодого возраста с выраженными клиническими проявлениями симпатикотонии. Среди лиц пожилого возраста они могут быть рекомендованы пациентам с сопутствующей стенокардией.
Диуретики наиболее показаны пациентам пожилого возраста, особенно при так называемой сользависимой артериальной гипертензии.
Показания к назначению кальциевых блокаторов существенно не отличаются от таковых к β-адреноблокаторам. У лиц с наклонностью к симпатикотонии предпочтение должно быть отдано изоптину, при брадикардии – коринфару или же дилтиазему. Кальциевые блокаторы должны рассматриваться как препараты выбора при лечении больных с сопутствующими сосудистыми заболеваниями (атеросклероз различной локализации с соответствующими клиническими проявлениями, синдром Рейно).
Ингибиторы системы ренин-ангиотензин особенно показаны больным с выраженной гипертрофией левого желудочка, сопутствующей ишемической болезнью сердца, сахарным диабетом и сердечной недостаточностью.
Вазодилататоры и α-адреноблокаторы редко используются в качестве единственного антигипертензивного средства. Они могут применяться у лиц среднего возраста без исходной тахикардии и с высокими значениями сосудистого сопротивления.
При назначении любого из препаратов должны быть учтены все противопоказания.
Монотерапия оправдана лишь у пациентов с умеренным повышением артериального давления. При наличии длительной и стойкой артериальной гипертензии целесообразно сразу же начинать комбинированную терапию. Вторым препаратом обычно является диуретик. Поводом для назначения третьего препарата является отсутствие должного ответа артериального давления на терапию двумя препаратами. У лиц с тяжелой артериальной гипертензией (диастолическое давление более 115 мм рт. ст.) изначально допустимо использование трех препаратов. Однако прием большого количества препаратов в течение дня психологически сложен для пациентов. Потому в подобных ситуациях целесообразно использовать медленно (длительно) действующие формы препаратов или же патентованные средства. У больных с тяжелой артериальной гипертензией нередко не удается нормализовать артериальное давление даже при назначении четырех антигипертензивных средств. Тем не менее даже умеренное снижение артериального давления существенно улучшает прогноз больных из-за уменьшения числа инсультов, сердечной недостаточности и замедления темпов прогрессирования заболевания.
Большая осторожность при проведении антигипертензивной терапии необходима у лиц пожилого возраста с сопутствующим атеросклерозом мозговых артерий или же ишемической болезнью сердца. Быстрая нормализация артериального давления у них нередко приводит к ухудшению самочувствия. Поэтому у таких больных необходимо постепенно снижать уровень артериального давления.
Поскольку гипертоническая болезнь – хроническое заболевание, то прекращение терапии закономерно приводит к повышению артериального давления. Поэтому задачей врача является подбор минимальных доз препаратов, позволяющих сохранять артериальное давление в нормальных пределах в течение многих лет.
Терапия гипертонических кризов. Появление у больного гипертонической болезнью клинической картины гипертонического криза является основанием для проведения неотложной терапии, направленной на снижение артериального давления. При этом выбор лекарственного препарата и темпы снижения артериального давления будут определяться двумя факторами: с одной стороны – особенностями течения криза (нейровегетативный, отечный, судорожный), с другой – наличием и выраженностью поражения органов-мишеней (проявления сердечной, цереброваскулярной и почечной недостаточности и др.). Наряду с этим на экстренность лечения будет влиять наличие и характер осложнений гипертонического криза (гипертоническая энцефалопатия, эклампсия, мозговой инсульт, острая коронарная и сердечная недостаточность, расслаивающая аневризма аорты).
Лечение неосложненного гипертонического криза может проводиться амбулаторно и только при сохранении картины криза, либо его осложненном течении, осуществляется госпитализация больного в стационар. Важнейшим принципом при лечении криза является постепенное снижение артериального давления, что позволит избежать (особенно у лиц старшего возраста) многочисленных осложнений, связанных с гипоперфузией мозга. Безопасным следует считать плавное снижение артериального давления в среднем на 25 % от исходного уровня, но не ниже 100 мм рт. ст. для диастолического артериального давления. Для купирования неосложненного гипертонического криза широко используются гипотензивные средства для приема внутрь (табл. 1.6). Хороший эффект оказывает прием 10 мг нифединина (коринфара). Быстро и эффективно снижает артериальное давление прием клофелина или каптоприла.
Таблица 1.6
Лекарственные препараты для купирования гипертонического криза
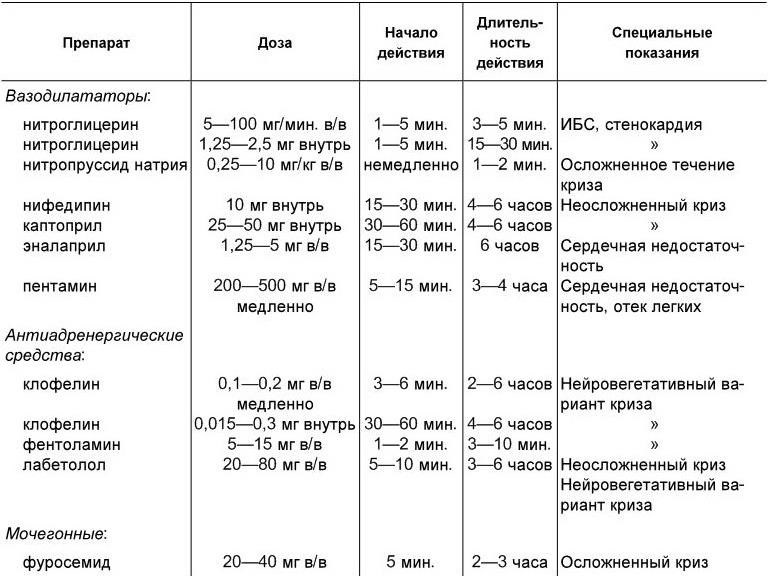
У больных ишемической болезнью сердца, имеющих проявления коронарной и сердечной недостаточности, хороший гипотензивный эффект наблюдается при сублингвальном приеме нитроглицерина.
Больные с клинической картиной осложненного гипертонического криза должны наблюдаться в отделении интенсивной терапии, где гипотензивные препараты вводятся внутривенно (см. табл. 1.6) под мониторным контролем АД. В процессе терапии гипертонического криза может возникнуть необходимость использования дополнительных лекарственных препаратов для купирования болевого синдрома (у больных ишемической болезнью сердца) и возбуждения (транквилизаторы), введение препаратов, улучшающих мозговое кровообращение и метаболизм миокарда.
После купирования гипертонического криза осуществляется подбор гипотензивной терапии с учетом обстоятельств его развития и предшествовавшей терапии.
Профилактика гипертонической болезни должна носить массовый характер и распространяться на все население. Основное направление профилактики – здоровый образ жизни (рациональное питание, достаточная физическая активность, сохранение нормальной массы тела, благоприятная психологическая обстановка и др.). Особенно пристальное внимание должно уделяться детям и подросткам, ближайшие кровные родственники которых имеют гипертоническую болезнь.
Все больные гипертонической болезнью должны находиться на диспансерном наблюдении. Желательно обучить больного измерению артериального давления, возможности адаптации дозы препаратов к его величинам. Успех терапии во многом определяется сознательным отношением больного к своему здоровью.
АТЕРОСКЛЕРОЗ
Определение. Атеросклероз – это хроническое заболевание артерий эластического и мышечно-эластического типа, характеризующееся отложением в интиме атерогенных апопротеин-В-содержащих липопротеидов с последующим разрастанием соединительной ткани и образованием фиброзных бляшек.
Распространенность. Атеросклероз встречается практически у всех людей. Первые липидные отложения выявляются уже у детей. В последующем их количество нарастает, что нередко приводит к появлению клинических симптомов.
Этиология. Возможность развития атеросклероза и скорость его прогрессирования определяются наличием факторов риска. Наиболее существенным из них является возраст (мужчины – старше 45 лет, женщины – старше 55 лет или же имеющие преждевременную менопаузу). В настоящее время клинические проявления атеросклероза у многих пациентов возникают в значительно более молодом возрасте. К числу других существенных факторов риска относятся наследственная предрасположенность, курение, артериальная гипертензия, дислипидемия, сахарный диабет. Несомненное отношение к развитию атеросклероза имеют гиподинамия, ожирение, гипофункция щитовидной железы и многие другие заболевания. Однако их не принято относить к основным факторам риска, поскольку влияние этих заболеваний на развитие атеросклероза связано с изменениями липидного обмена и/или функционального состояния эндотелия. Чем больше факторов риска имеет человек, тем выше у него возможность развития атеросклероза в молодом возрасте.
Патогенез. Возможность развития атеросклероза определяется взаимодействием нескольких механизмов, наиболее существенными из которых являются нарушения метаболизма липидов (дислипидемия), состояние сосудистой стенки (преимущественно, эндотелия), а также функциональная активность макрофагов, тромбоцитов и некоторых других клеток.
Начало изучения роли дислипидемии как важнейшего фактора патогенеза атеросклероза положили блестящие экспериментальные исследования Н. Е. Аничкова и С. С. Халатова (1912) по воспроизведению атеросклероза у кроликов при скармливании им большого количества холестерина. Многочисленные клинические исследования, выполненные в последующие годы, показали, что уровень общего холестерина в крови является одним из существенных факторов риска развития атеросклероза.
К числу биохимических факторов риска развития атеросклероза относится и гипертриглицеридемия. Поэтому принято выделять нормальные, пограничные и высокие значения холестерина и триглицеридов (табл. 1.7).
Таблица 1.7
Содержание холестерина и триглицеридов в крови

Человек в сутки получает с пищей около 300 – 400 мг холестерина и около 700 мг холестерина синтезируется в печени. Минимальное количество холестерина синтезируется в кишечнике и в почках. В течение суток около 450 мг холестерина превращается в желчные кислоты, такое же количество стеринов удаляется с фекалиями, небольшая часть холестерина удаляется из организма сальными железами и идет на синтез гормонов. Триглицериды (нейтральные жиры) синтезируются в печени и в кишечной стенке.
В крови холестерин и триглицериды циркулируют в виде сферических макромолекуляных комплексов (частиц), содержащих также фосфолипиды, белки и эфиры холестерина (липопротеиды). Эти частицы в соответствии с размерами и плотностью подразделяются на пять основных классов. Самые крупные из них — хиломикроны – переносят триглицериды и небольшое количество холестерина из стенки кишечника в кровь. Синтезированный в печени холестерин поступает в кровь в составе липопротеидов очень низкой плотности (ЛПОНП). В крови под влиянием липопротеидлипазы, локализованной, преимущественно, на эндотелии, липопротеиды очень низкой плотности расщепляются до липопротеидов промежуточной плотности (ЛППП). Липопротеиды промежуточной плотности под влиянием печеночной липопротеидлипазы превращаются в липопротеиды низкой плотности (ЛПНП). Липопротеиды низкой плотности содержат максимальное количество холестерина и являются наиболее атерогенными. Они интенсивно захватываются печеночными клетками и периферическими тканями, в том числе макрофагами (рис. 1.2). Поступление липопротеидов низкой и промежуточной плотности в печеночную клетку – рецепторопосредованный процесс. Количество рецепторов в печеночной клетке в значительной мере генетически детерминировано, и при их недостатке возникает один из вариантов наследственной гиперхолестеринемии. В печени из липопротеидов низкой плотности образуются липопротеиды высокой плотности (ЛПВП). Кроме того, значительная часть холестерина липопротеидов промежуточной и низкой плотности в печеночной клетке метаболизируется до желчных кислот и поступает в кишечник. Липопротеиды высокой плотности обладают антиатерогенным действием, поскольку они способны захватывать холестерин в тканях (клетках) и удалять его (обратный транспорт холестерина). Кроме того, липопротеидам высокой плотности присуща антиоксидантная активность, препятствующая перекисному окислению ЛПНП. Поскольку ЛПВП обладают антиатерогенными свойствами, то их взаимоотношение с другими классами липопротеидов в определяющей мере формирует атерогенный потенциал крови.
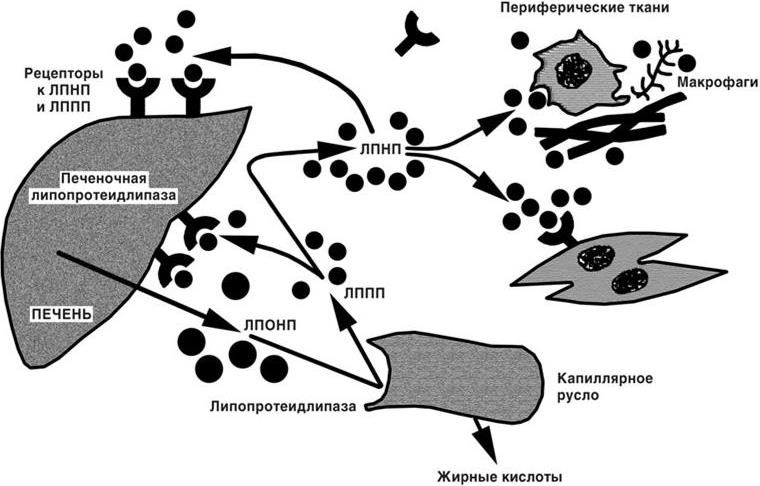
Рис. 1.2. Обмен эндогенных липопротеидов (объяснения в тексте)
Степень этих нарушений оценивается различными коэффициентами атерогенности. Наиболее часто используется формула, предложенная А. Н. Климовым. Коэффициент атерогенности (КА) рассчитывается следующим образом:
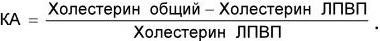
Нормальными являются показатели, не превышающие 3.
Уровень атерогенности липопротеидов определяется и характером гликопротеидов, входящих в состав этих частиц. Идентифицировано несколько типов гликопротеидов, входящих в состав липопротеидов (anoA, anoB, anoC, anoD, anoE и ano(a)). Апопротеиды являются своеобразными активными участками липопротеидных частиц. Они обеспечивают соединение частиц с рецепторами клеток, изменяют активность многих ферментов, участвующих в переносе и метаболизме холестерина и триглицеридов. Наиболее атерогенными являются комплексы, содержащие anoB и ano(a), входящие в состав липопротеидов низкой плотности. Это связано с низким количеством рецепторов к данному типу гликопротеидов в печеночной клетке, что в значительной степени генетически обусловлено. В то же время комплексы липопротеидов, имеющие в своем составе anoA (ЛПВП), обладают выраженными антиатеросклеротическими свойствами.
С учетом содержания в крови общего холестерина, холестерина липопротеидов низкой плотности и триглицеридов Фредриксоном была предложена классификация гиперлипидемий, принятая ВОЗ (табл. 1.8). Наиболее атерогенным и часто встречающимся является II тип гиперлипопротеидемии, что в значительной мере обусловлено преимущественным увеличением в плазме концентрации холестерина липопротеидов низкой плотности.
Таблица 1.8
Классификация гиперлипопротеидемий
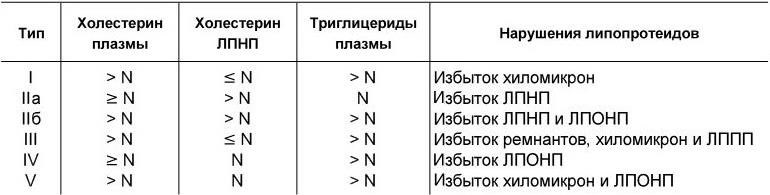
Риск развития атеросклероза обусловлен не только характером изменений состава липопротеидов плазмы. Наибольшей атерогенностью обладают не нативные, а измененные (модифицированные) липопротеиды. Одной из наиболее частых причин модификации липопротеидов является их перекисное окисление. Атерогенность модифицированных липопротеидов может быть обусловлена многими причинами, среди которых наиболее доказанными являются две. Во-первых, это нарушение утилизации модифицированных липопротеидов макрофагами. Чувствительность рецепторов к немодифицированным липопротеидам регулируется по принципу обратной связи. Поэтому при достижении ими определенной концентрации в цитоплазме макрофагов дальнейший захват прекращается, и имеющийся в клетке холестерин частично используется для возобновления клеточных мембран, частично метаболизируется. В то же время при поступлении в макрофаг модифицированных липопротеидов принцип обратной связи нарушается. В результате макрофаг оказывается перегруженным липопротеидами и превращается в типичную пенистую клетку, которая со временем разрушается. При этом во внеклеточное пространство поступает холестерин, его эфиры, а также различные биологически активные вещества. Второй механизм атерогенного действия модифицированных липопротеидов обусловлен изменениями состава белков и приобретением ими антигенных свойств, что стимулирует выработку специфических антител и последующее повреждение эндотелия и тромбоцитов циркулирующими иммунными комплексами.
Таким образом, возникновение атеросклеротических изменений сопряжено с целым рядом существенных изменений липидного состава плазмы крови. Липопротеиды постоянно фильтруются из крови в ткани через сосудистую стенку. Скорость их поступления в сосудистую стенку в решающей мере определяется состоянием эндотелия. Липопротеиды могут проходить через эндотелий как посредством обычной фильтрации (диффузии), так и с помощью эндоцитоза. Поэтому любое повреждение эндотелия может способствовать увеличению количества липопротеидов, поступающих в сосудистую стенку.
Функциональное состояние эндотелия могут изменять очень многие воздействия. Наиболее существенными из них являются артериальная гипертензия, курение, циркулирующие иммунные комплексы. Токсическое действие на эндотелий оказывают модифицированные липопротеиды, свободные радикалы. Установлено неблагоприятное влияние на него катехоламинов, ангиотензина-II, вирусов и многих биологически активных веществ.
Повреждение эндотелия приводит к скоплению на его поверхности моноцитов и тромбоцитов. Моноциты проникают под эндотелий, захватывают большое количество липопротеидов и превращаются в пенистые клетки. Поврежденный эндотелий, макрофаги и адгезированные тромбоциты выделяют большое количество биологически активных веществ, изменяющих состояние сосудистой стенки, стимулирующих пролиферацию гладкомышечных клеток и их миграцию к очагу повреждения. Кроме того, под влиянием этих факторов гладкие мышцы приобретают способность к синтезу основных компонентов соединительной ткани.
Часть пенистых клеток постепенно разрушается, и содержащиеся в них холестерин и его эфиры оказываются вне клеток, образуя «липидное ядро» будущей бляшки, которое постепенно покрывается соединительнотканными элементами, гладкомышечными клетками и эндотелием.
Морфология. Неосложненная атеросклеротическая бляшка имеет покрышку, состоящую из элементов соединительной ткани, гладкомышечных клеток, покрытых эндотелием. Холестерин и его эфиры, а также пенистые клетки (макрофаги) содержатся в центре бляшки (рис. 1.3). Постепенно в бляшках откладывается кальций.
Состояние бляшки не является стабильным. Возможны надрывы и изъязвление покрышки, кровоизлияния в бляшку. Эти изменения обычно приводят к обострению заболеваний, обусловленных атеросклерозом (ишемическая болезнь сердца, мозга).
Клиническая картина. Клинические проявления атеросклероза определяются локализацией морфологических изменений. Далеко не все сосуды поражаются атеросклерозом в одинаковой степени. Наиболее часто изменения развиваются в коронарных, мозговых, почечных артериях, артериях нижних конечностей и в аорте. Исключительно редко изменения выявляются в легочной артерии. Атеросклероз коронарных артерий проявляется ишемической болезнью сердца, мозговых – мозга, почек – вазоренальной артериальной гипертензией. Клинические проявления могут быть обусловлены спазмом артерий, их тромбозом в области измененной бляшки (инфаркт миокарда, синдром Лериша и др.), симптомами, связанными с хронической недостаточностью кровообращения из-за сужения просвета артерии (стенокардия напряжения, перемежающаяся хромота), эмболиями, возникающими в местах сужения артерий из-за турбулентного тока крови и образования тромбов в области измененных артерий (сонные артерии – эмболии в мозг). При распространенных атеросклеротических изменениях аорты и крупных артерий возможно образование аневризм. Резкое расширение восходящего отдела аорты обычно сочетается с расширением кольца аортального клапана и формированием его недостаточности.
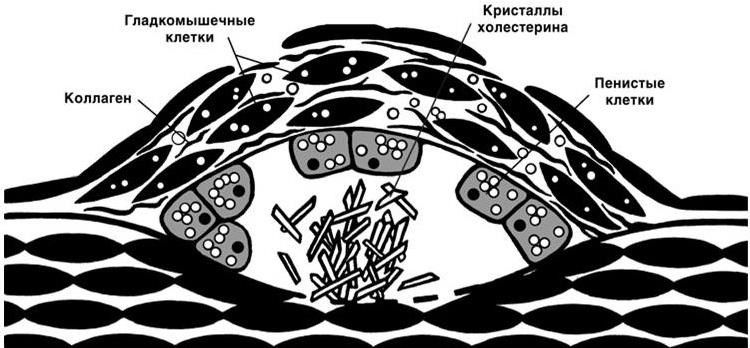
Рис. 1.3. Схема атеросклеротической бляшки (по G. R. Thompson)
В редких случаях, чаще при семейных (наследственных) дислипидемиях, липиды откладываются в области Ахиллова и других сухожилий (ксантомы сухожилий), вокруг глаз (ксантелазмы), в роговице (сенильное кольцо, липоидная дуга роговицы).
Лабораторная и инструментальная диагностика. При подозрении на наличие атеросклероза у части больных выявляются характерные изменения липидного спектра крови (см. патогенез). Однако нормальный спектр липидов не отрицает диагноза атеросклероза.
Аневризма грудного отдела аорты выявляется при рентгенологическом исследовании. Для визуализации атеросклероза крупных и средних артерий возможно использование ультразвукового метода. В последние годы разработаны специальные ультразвуковые внутрисосудистые датчики, в том числе и для исследования коронарных артерий. Однако метод внутрисосудистого ультразвукового исследования не нашел широкого распространения из-за его дороговизны и инвазивного характера.