Проектирование медицинских изделий
1.4 Процедура регистрация медицинских изделий в ЕАЭС
Сначала обратимся к основным понятиям и главным участникам процедуры регистрации продукции на основании требований Евразийского экономического союза. Регистрация медицинского изделия – процедура выдачи уполномоченным органом референтного государства разрешения на выпуск в обращение медицинского изделия на территории одного или нескольких государств-членов.
Документ выдается уполномоченным органом в форме регистрационного удостоверения, которое подтверждает прохождение регистрационной процедуры медицинским изделием.
Референтное государство – выбранное заявителем государство-член ЕАЭС, уполномоченный орган которого осуществляет регистрацию медицинского изделия. Государство признания – государство-член, уполномоченный орган (экспертная организация) которого осуществляет процедуру согласования экспертного заключения референтного государства.
В общем виде механизм регистрации медицинского изделия в рамках Евразийского экономического союза выглядит так:
– Заявитель знакомится с требованиями законодательства для своего изделия.
– Затем он с привлечением уполномоченных испытательных организаций проходит испытания, предусмотренные для этой категории изделий, и получает протоколы по их результатам.
– Заявитель выбирает референтное государство, то есть страну, в которой будет проводиться процедура государственной регистрации. Также на этом этапе ему нужно будет выбрать государства признания, то есть страны, в которых будет действовать полученное регистрационное удостоверение.
– Подготовленное досье подается в регистрирующий орган, действующий в референтном государстве. В Российской Федерации эту функцию выполняет Росздравнадзор.
– Уполномоченный государственный орган с привлечением экспертной организации проводит экспертизу качества, эффективности и безопасности изделия, представленного на регистрацию.
– Уполномоченный государственный орган референтного государства размещает готовое экспертное заключение в единой информационной системе для ознакомления и согласования с государствами признания.
– По результатам согласования заключения государствами признания уполномоченный орган выносит окончательное решение о регистрации изделия.
– Информация о выданном документе вносится в Единый реестр зарегистрированных медицинских товаров Евразийского экономического союза. В Российской Федерации эту процедуру выполняет Росздравнадзор.
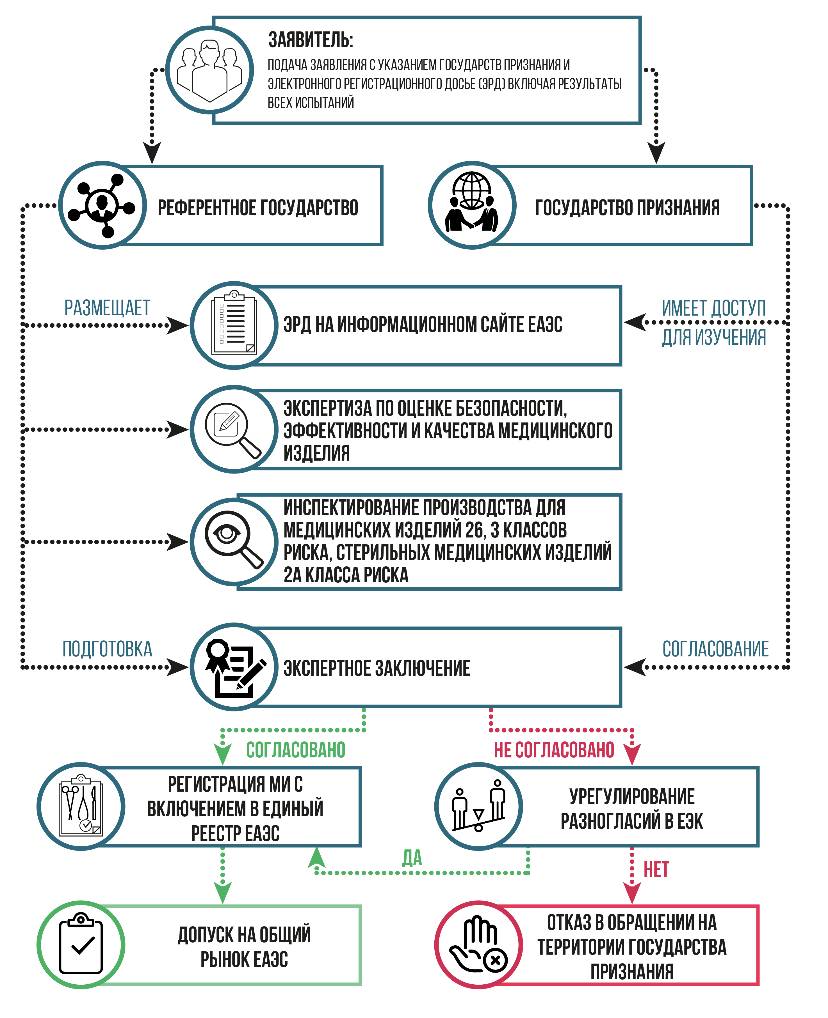
Рисунок 1.2 – Регистрация медицинских изделий в ЕАЭС
Важно знать, что заявитель/обладатель регистрационного удостоверения повсеместно известен как производитель. Он является вершиной регулирующей цепи и несет полную ответственность за безопасность указанного изделия; дизайнер, субподрядчик, упаковщик и т. д. подчиняются ему. Однако все они являются частью процесса регулирования. Со статусом производителя появляются уровни ответственности, выходящие за рамки простого страхования, такие как отчетность, послепродажное наблюдение, сбор клинических данных и многое другое.
РЕЗЮМЕ
Проектирование и разработка медицинского изделия является наиболее важным этапом для его успеха. Медицинское изделие с нечетким назначением и дизайном не может соответствовать нормативным требованиям и выйти на рынок. Требуются значительные усилия, чтобы предоставить правильное решение для здравоохранения, отвечающее требованиям потребителей. Правильное решение для здравоохранения требует, чтобы была четко определены область применения изделия в соответствии с потребностями конечного пользователя, требования спецификации изделия, минимальные риски использования и максимально возможное качество.
Учитывая это, мы подготовили это пособие по проектированию и разработке медицинских изделий. Во введении были обозначены основные регуляторные органы и прописаны нормативные акты, которые контролируют среду медицинских изделий. Важно знать, что медицинские изделия – это строго регулируемая сфера, поэтому любая дизайнерская работа должна быть на должном уровне.

1. Опишите чем процедура регистрации медицинских изделий в Российской Федерации отличается от регистрации в Евразийском экономическом союзе.
2. Чем отличаются медицинские изделия для диагностики in vitro от медицинских изделий.
3. Как определить являются ли разрабатываемое изделие медицинским или нет?
4. Являются ли часы, которые показывают пульс пользователя медицинским изделием? В каком случае они будут являться медицинским изделием?
5. Чем дизайн (проектирования) изделия отличается от инжиниринга?


1. Федеральный закон от 21 ноября 2011 г. №323 ФЗ "Об основах охраны здоровья граждан в Российской Федерации,статья 38.
2. Решение Совета Евразийской экономической комиссии от 24 декабря 2021 г. N 144 «О внесении изменений в Правила регистрации и экспертизы безопасности, качества и эффективности медицинских изделий».
3. Постановление Правительства Российской Федерации от 27 декабря 2012 г. № 1416
«Об утверждении Правил государственной регистрации медицинских изделий».
4. Постановление Правительства РФ от 3 апреля 2020 г. № 430 "Об особенностях обращения медицинских изделий, в том числе государственной регистрации серии (партии) медицинского изделия.
5. Постановление Правительства РФ от 1 апреля 2022 г. № 552 "Об утверждении особенностей обращения, включая особенности государственной регистрации, медицинских изделий в случае их дефектуры или риска возникновения дефектуры в связи с введением в отношении Российской Федерации ограничительных мер экономического характера.

02 Классификация медицинских изделий
2.1 Зачем классифицировать?
Существует ряд причин, по которым классификация важна.
Первая причина касается пациента. Не все изделия представляют собой одинаковый риск, рассмотрим, например, кардиостимулятор и поддерживающую повязку. Очевидно, что кардиостимулятор представляет больший риск и, следовательно, должен иметь более строгий контроль, связанный с его конструкцией, производством и возможными продажами.
Вторая причина касается производителя; очевидно, что требования к регистрации поддерживающей повязки должны отличаться от кардиостимулятора?
Третья причина касается регулирующих органов; классификация указывает им уровень риска для пациента и, следовательно, количество усилий, которые им необходимо приложить для контроля
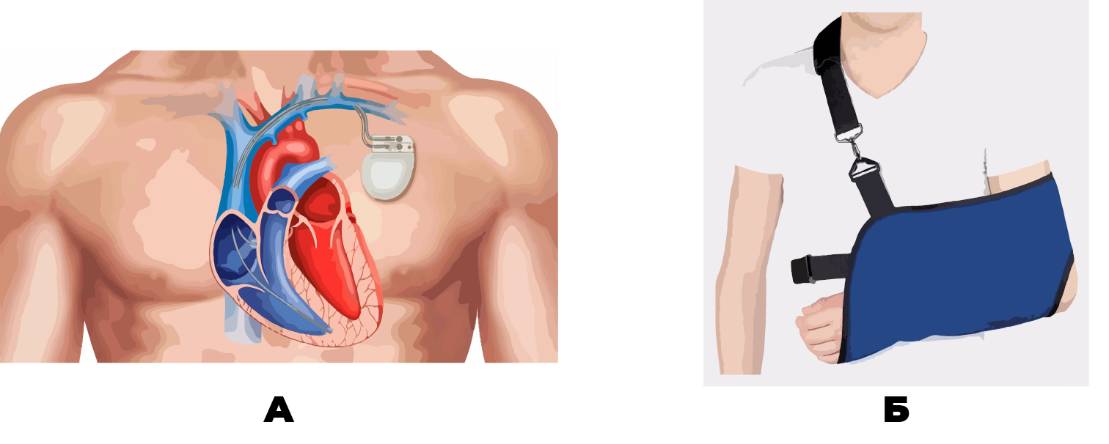
Рисунок 2.1 – А. Электрокардиостимулятор. Б. Поддерживающая повязка.
А. Электрокардиостимулятор – медицинский прибор, предназначенный для воздействия на ритм сердца. Основной задачей кардиостимулятора является поддержание или навязывание частоты сердечных сокращений пациенту, у которого сердце бьётся недостаточно часто или имеется электрофизиологическое разобщение между предсердиями и желудочками.
Б. Поддерживающая повязка – это повязка, которая используется для поддержания травмированной руки.
Безусловно, первостепенное значение имеет безопасность. Все изделия должны соответствовать основному критерию «не навреди». Однако для некоторых изделий для достижения клинической цели неизбежен некоторый вред. Возникает вопрос: «Приемлем ли риск?». Рассмотрим, например, иглу для подкожных инъекций. Что наносит больший вред: нанесение небольшой колотой ранки на кожу или отказ от прививки? Риск и непричинение вреда – это баланс. Поэтому «потенциальный риск применения» медицинского изделия определяется как комбинация вероятности причинения вреда при применении медицинских изделий в соответствии с назначением, определенным производителем, и тяжести этого вреда. Классификация позволяет всем участникам процесса регулирования понять риск, который представляет изделие. В целом, чем выше класс риска, тем больше шансов, что изделие может нанести какой-то вред. Поэтому неудивительно, что такие изделия, как сердечные клапаны, имеют более высокий класс риска, чем вставки для обуви.
Классификации основаны на риске для пациента. Важно отметить, что риск является очень важным аспектом управления дизайном; понимание риска для пациента (и клинической бригады/оператора) имеет основополагающее значение.
Прежде чем идти дальше, нужно обозначить некоторые определения2:
2.2 Термины и определения
Активные диагностические медицинские изделия – активные медицинские изделия, предназначенные для представления информации в целях диагностики, контроля лечения или изменения физиологического состояния, состояния заболевания или врожденных дефектов;
Активные медицинские изделия – медицинские изделия, применяемые отдельно или в сочетании с другими медицинскими изделиями, для действия которых необходимо использование энергии, отличной от производимой человеком, или силы тяжести.
Медицинские изделия, предназначенные для передачи энергии или веществ от активного медицинского изделия к пациенту без их существенного изменения, не являются активными медицинскими изделиями. Самостоятельное программное обеспечение рассматривается как активное медицинское изделие;
Активные терапевтические медицинские изделия – активные медицинские изделия, предназначенные для сохранения, изменения, замены или восстановления биологических функций или структур, связанных с лечением, облегчением болезни, ранением или инвалидностью;
Вред – травмирование или нанесение ущерба здоровью человека, оборудованию или окружающей среде;
Имплантируемые медицинские изделия – инвазивные медицинские изделия, в том числе частично или полностью рассасывающиеся в организме, полностью вводимые в тело человека или заменяющие эпителиальную поверхность или поверхность глаза посредством хирургического вмешательства и остающиеся в месте введения после хирургической процедуры, а также медицинские изделия, частично вводимые в тело человека посредством хирургического вмешательства и остающиеся в месте введения после хирургической процедуры более 30 суток;
Инвазивные медицинские изделия – медицинские изделия, предназначенные для полного или частичного введения в тело человека через его поверхность либо через отверстие тела;
Медицинские изделия для временного применения – медицинские изделия, предназначенные для непрерывного применения от 60 минут до 30 суток в соответствии с инструкцией по применению или руководством по эксплуатации;
Медицинские изделия для длительного применения – медицинские изделия, предназначенные для непрерывного применения в течение более 30 суток в соответствии с инструкцией по применению или руководством по эксплуатации;
Медицинские изделия для кратковременного применения – медицинские изделия, предназначенные для непрерывного применения в течение не более 60 минут в соответствии с инструкцией по применению или руководством по эксплуатации;
Назначение медицинского изделия – документированное решение производителя в отношении целевого использования медицинского изделия, основанное на его свойствах, отраженных в технических характеристиках, инструкции по применению или руководстве по эксплуатации;
Наноматериал – материал, который содержит частицы, находящиеся в несвязанном состоянии, либо частицы в виде агрегатов или агломератов и в котором не менее 50 процентов частиц имеют размеры в диапазоне 1…100 нм. При этом под агрегатами понимаются частицы, состоящие из сплавленных или прочно связанных частиц, под агломератами – объединения слабо связанных частиц. К наноматериалам также относятся частицы графена или углеродные нанотрубки с одним или несколькими внешними размерами меньше 1 нм;
Неинвазивные медицинские изделия – медицинские изделия, не предназначенные для полного или частичного введения в тело человека через его поверхность либо через отверстие тела;
Отверстие тела – любое естественное отверстие в теле человека, а также внешняя поверхность глазного яблока или любое постоянное искусственное отверстие (полость);
Потенциальный риск применения – комбинация вероятности причинения вреда при применении медицинских изделий в соответствии с назначением, определенным производителем, и тяжести этого вреда;
Хирургические инвазивные медицинские изделия – инвазивные медицинские изделия, полностью или частично вводимые в тело человека через его поверхность или через отверстие тела путем хирургического вмешательства или в связи с ним
Эти определения универсальны и важны. На первых страницах нормативных документов (например, Постановления, приказы и т.п.) обычно прописаны определения терминов. Они необходимы для того, чтобы все участники процесса (производители, регистрирующие органы, пользователи) говорили на одном языке.
2.3 Есть ли правила классификации медицинских изделий в зависимости от риска?
Класс потенциального риска применения в Российской Федерации регламентируется Приказом Министерства здравоохранения РФ от 6 июня 2012 г. N 4н "Об утверждении номенклатурной классификации медицинских изделий" (с изменениями и дополнениями), а в ЕАЭС – Решением Коллегии Евразийской экономической комиссии от 22 декабря 2015 г. N 173 «Об утверждении Правил классификации медицинских изделий в зависимости от потенциального риска применения».
В Российской Федерации и ЕАЭС классификация медицинских изделий происходит по одному принципу. Медицинские изделия в зависимости от степени потенциального риска применения подразделяются на 4 класса. Классы имеют обозначения 1, 2а, 2б и 3.
Каждое медицинское изделие может быть отнесено только к одному классу:
Класс 1 – медицинские изделия с низкой степенью риска.
Класс 2а – медицинские изделия со средней степенью риска. Класс 2б – медицинские изделия с повышенной степенью риска. Класс 3 – медицинские изделия с высокой степенью риска.
Также при классификации медицинских изделий для диагностики in vitro (ИВД) каждое медицинское изделие может быть отнесено только к одному классу:
к классу 1 – относятся медицинские изделия для диагностики in vitro с низкой степенью потенциального риска применения для отдельного человека и низкой степенью потенциального риска применения для общественного здоровья;
к классу 2а – медицинские изделия для диагностики in vitro со средней степенью потенциального риска применения для отдельного человека и низкой степенью потенциального риска применения для общественного здоровья;
к классу 2б – медицинские изделия для диагностики in vitro с высокой степенью потенциального риска применения для отдельного человека и (или) средней степенью потенциального риска применения для общественного здоровья;
к классу 3 – медицинские изделия для диагностики in vitro с высокой степенью потенциального риска применения для отдельного человека и высокой степенью потенциального риска применения для общественного здоровья.
2.4 Основные правила классификации медицинских изделий
3
До классификации медицинского изделия, производитель прежде всего должен:
1. Решить, является ли рассматриваемый продукт медицинским изделием, используя соответствующее определение.
2. Определить предполагаемое использование медицинского изделия.
3. Принять во внимание все приведенные ниже правила, чтобы установить надлежащую классификацию изделия, отметив, что, если медицинское изделие имеет характеристики, которые относят его более чем к одному классу, классификация и оценка соответствия должны основываться на самом высоком указанном классе.
Фактическая классификация каждого изделия зависит от точных заявлений производителя и его предполагаемого использования. Хотя предоставление примеров ниже полезно при интерпретации цели каждого правила, необходимо подчеркнуть, что фактические классификация конкретного изделия должна рассматриваться индивидуально с учетом его конструкции и предполагаемого использования.
2.4.1 Классификация неинвазивных медицинских изделий
Эти правила применяются в целом к изделиям, которые вступают в контакт только с неповрежденной кожей или не вступают в непосредственный контакт с пациентом.
1. Неинвазивные медицинские изделия относятся к классу 1, если в отношении их не применяются пункты, изложенные далее (например, больничные койки, подъемники для пациентов).
2. Неинвазивные медицинские изделия, предназначенные для хранения органов, частей органов либо хранения или введения в организм человека крови, других жидкостей, газов, паров или тканей, относятся к классу 2а, в том числе в случае их использования совместно с активными медицинскими изделиями класса 2а или более высокого класса (например, шприцы для инфузионных насосов).
3. Неинвазивные медицинские изделия, предназначенные для изменения биологического или физико-химического состава и свойств крови, тканей, клеток, других физиологических жидкостей или жидкостей, которые должны поступать в организм, относятся к классу 2б (например, изделия, предназначенные для удаления нежелательных веществ из крови путем обмена растворенных веществ, такие как гемодиализаторы). Однако, если их действие заключается только в фильтрации от частиц, обработке на центрифуге, газо- или теплообмене, указанные медицинские изделия относятся к классу 2а (например, изделия для подогрева или охлаждения крови).
4. Неинвазивные медицинские изделия, которые соприкасаются с поврежденной кожей, относятся:
а) к классу 1 – если они используются как механические барьеры, для компрессии или абсорбции экссудатов (например, вата, раневые полоски);
б) к классу 2б – если они используются для ран, которые можно залечить только посредством вторичного заживления (например, повязки для сильных ожогов);
в) к классу 2а – в иных случаях (в том числе в случае, если медицинские изделия предназначены преимущественно для воздействия на микросреду ран) (например, марлевые повязки, пропитанные нелекарственными препаратами).
2.4.2 Классификация инвазивных медицинских изделий
Такие изделия являются инвазивными в отношении отверстий тела (см. определение) и не являются хирургически инвазивными. Для краткосрочного использования необходимо провести дополнительное различие между инвазивностью в отношении менее уязвимых частей уха, рта и носа и других анатомических участков, к которым можно получить доступ через естественные отверстия тела. Хирургически созданная стома, которая, например, позволяет эвакуировать мочу или фекалии, также считается отверстием тела.
Изделия, на которые распространяется это правило, как правило, являются диагностическими и терапевтическими инструментами, используемыми в определенных областях (оториноларингология, офтальмология, стоматология, проктология, урология и гинекология). Классификация зависит от времени инвазии и чувствительности (или уязвимости) тела к такой инвазии.
5. Инвазивные медицинские изделия (за исключением хирургических инвазивных), применение которых связано с отверстиями тела и которые не предназначены для присоединения к активному медицинскому изделию или предназначены для присоединения к активному медицинскому изделию класса 1, относятся:
а) к классу 1 – если это медицинские изделия для кратковременного применения (например, смотровые перчатки);
б) к классу 2а – если это медицинские изделия для временного применения (например, эндотрахеальные трубки). Однако, если указанные медицинские изделия временно применяются в полости рта до глотки, в слуховом проходе до барабанной перепонки или в полости носа, они относятся к классу 1 (например, зубные протезы, предназначенные для снятия пациентом);
в) к классу 2б – если это медицинские изделия для длительного применения (например, уретральный стент). Однако, если указанные медицинские изделия длительно применяются в полости рта до глотки, в слуховом проходе до барабанной перепонки или в полости носа и не могут быть абсорбируемы слизистой оболочкой, они относятся к классу 2а (например, несъемный зубной протез).
Инвазивные медицинские изделия (за исключением хирургических инвазивных), применение которых связано с отверстиями тела и которые предназначены для присоединения к активному медицинскому изделию класса 2а или более высокого класса, относятся к классу 2а (отсасывающие катетеры для дренирования желудка).
Хирургические инвазивные медицинские изделия
6. Хирургические инвазивные медицинские изделия для кратковременного применения относятся к классу 2а (например, иглы или шприцы) за исключением следующих случаев:
а) если указанные медицинские изделия предназначены для диагностики, наблюдения, контроля или коррекции патологий сердца, центральной системы кровообращения или центральной нервной системы в прямом контакте с органами или частями этих систем, они относятся к классу 3 (например, сердечно-сосудистые катетеры);
б) если указанные медицинские изделия являются многоразовыми хирургическими инструментами, они относятся к классу 1 (например, ретракторы грудины для временного использования);
в) если указанные медицинские изделия предназначены для передачи энергии в форме ионизирующего излучения, они относятся к классу 2б (например, катетеры, содержащие или включающие радиоизотопы);
г) если указанные медицинские изделия предназначены для того, чтобы вызывать биологический эффект либо рассасываться полностью или в значительной мере, они относятся к классу 2б (например, вязкоупругий раствор для офтальмологической хирургии);
д) если указанные медицинские изделия предназначены для введения лекарственных препаратов непрофессиональными пользователями, они относятся к классу 2б (например, инсулиновая ручка для самостоятельного введения).
7. Хирургические инвазивные медицинские изделия для временного применения относятся к классу 2а (например, временные пломбировочные материалы), за исключением следующих случаев:
а) если указанные медицинские изделия предназначены для диагностики, наблюдения, контроля или коррекции патологий сердца или центральной системы кровообращения в прямом контакте с органами или частями этих систем, они относятся к классу 3 (например, датчики сердечного выброса);
б) если указанные медицинские изделия непосредственно контактируют с центральной нервной системой, они относятся к классу 3 (например, неврологические катетеры);
в) если указанные медицинские изделия предназначены для передачи энергии в форме ионизирующего излучения, они относятся к классу 2б (например, устройство для брахитерапии);
г) если указанные медицинские изделия предназначены для того, чтобы вызывать биологический эффект либо рассасываться полностью или в значительной мере, они относятся к классу 3 (например, биологический клей);
д) если указанные медицинские изделия претерпевают в теле человека химические изменения, они относятся к классу 2б (за исключением медицинских изделий, предназначенных для имплантации в зубы или для введения лекарственных препаратов) (например, гемостатические пены).
8. Имплантируемые4 медицинские изделия, а также хирургические инвазивные медицинские изделия для длительного применения относятся к классу 2б (например, катетеры для периферических сосудов для длительного использования), за исключением следующих случаев:
а) если указанные медицинские изделия предназначены для имплантации в зубы, они относятся к классу 2а (например, мосты и коронки);