
Химия для студентов-медиков: общая, физическая и коллоидная химия. Практикум-рабочая тетрадь
• Молекулы имеют определенное химическое строение, под которым подразумевают порядок связей атомов в молекуле.
• Свойства молекулы определяются её химическим строением и природой образующих её атомов.
• Изучая химические превращения вещества, можно установить его химическое строение.
Электронная теория химической связи сформировалась только в 20-х годах XX века. Квантовая химия описывает химическую связь как результат электростатического взаимодействия между валентными электронами и положительно заряженными ядрами взаимодействующих атомов. Это взаимодействие обязательно должно приводить к уменьшению общей энергии системы, т.е. должно быть энергетически выгодно.
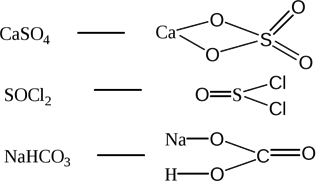
Ионная связь образуется за счёт электростатического притяжения разнозаряженных ионов, образующихся при полном смещении общей электронной плотности к более электроотрицательному атому. Такая химическая связь возникает между элементами резко отличающимися по электроотрицательности (более 1,5 по шкале Полинга), например, между элементами IА и VIIА подгрупп.
Ковалентная химическая связь образуется за счёт формирования общей (связывающей) электронной пары между взаимодействующими атомами. Например, в молекуле водорода одна связывающая электронная пара Н : Н. Такую связь называют одинарной. Возникновение кратной связи (двойной или тройной) равносильно образованию двух или трёх общих электронных пар.
Неполярная ковалентная связь образуется в простых веществах молекулярного или кристаллического строения между атомами одного элемента. В этом случае общая электронная плотность находится строго симметрично относительно связанных атомов. Поэтому поляризация атомов в молекулах или кристаллах простых веществ отсутствует.
Полярная ковалентная связь образуется в сложных веществах между разными по электроотрицательности атомами. При образовании полярной ковалентной связи общая электронная плотность смещается к более электроотрицательному атому. Это равносильно возникновению у атомов частичных электрических зарядов.
Металлическая химическая связь образуется за счёт обобществления валентных электронов атомов, образующих кристаллическую решетку – это многоцентровая химическая связь с дефицитом электронов. По своей природе она похожа на ковалентную неполярную или слабо полярную связь, но в отличие от неё является ненаправленной. Металлическая связь встречается в кристаллах металлов и металлоподобных веществ.
Степень окисления – это условный заряд атома, показывающий количество отданных или принятых им электронов, при образовании ионных связей в молекуле или ионе. Степень окисления атомов в простых веществах равна нулю. Высшая степень окисления атома для элементов главных подгрупп периодической системы совпадает с номером группы. Низшая (отрицательная) степень окисления возникает у наиболее электроотрицательных атомов в молекуле при присоединении электронов. Её можно вычислить, если из восьми вычесть номер группы, в которой расположен элемент.
Примеры степеней окисления элементов:
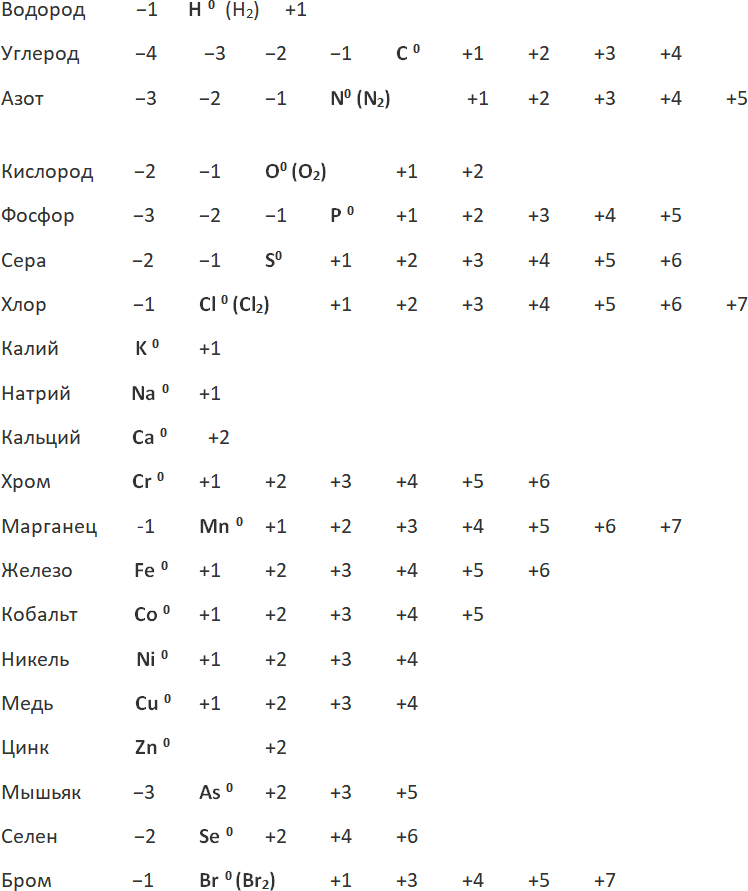
Основные характеристики химической связи – прочность, длина, полярность, устойчивость.
При образовании химической связи энергия выделяется, при ее разрыве – поглощается. Энергия, необходимая для того чтобы разъединить атомы и удалить их друг от друга на расстояние, на котором они не взаимодействуют, называется энергией связи. Важными характеристиками химической связи являются также ее длина и кратность.
Длина связи определяется расстоянием между ядрами связанных атомов в молекуле. Как правило, длина химической связи меньше, чем сумма радиусов атомов, за счет перекрывания электронных облаков.
Кратность связи определяется количеством электронных пар, связывающих два атома.
Свойства ковалентной связи: насыщаемость, направленность и поляризуемость.
• Насыщаемость ковалентной связи обусловлена ограниченными валентными возможностями атомов, т.е их способностью к образованию строго определенного числа связей, которое обычно лежит в пределах от 3 до 80.
• Направленность ковалентной связи является результатом стремления атомов к образованию наиболее прочной связи за счет возможно большей электронной плотности между ядрами.
• Поляризуемость рассматривают на основе представлений о том, что ковалентная связь может быть неполярной (чисто ковалентной) или полярной.
1.2. СтехиометрияСтехиометрия – раздел химии, устанавливающий правила расчета по химическим формулам веществ, уравнениям химических реакций, правила вычислений при приготовлении, разбавлении и смешении растворов, правила обработки результатов количественного химического анализа.
Каждое вещество имеет строго определенный элементный состав, который отражает его структурная единица. Для веществ молекулярной природы (газы, жидкости, молекулярные кристаллы) в качестве структурной единицы выступает реальная частица – молекула. Для простых веществ с атомной структурой (металлы, алмаз, графит и др.) структурной единицей является атом.
Для сложных кристаллических веществ, имеющих ионную решетку (соли, основания) или решетку с ковалентными полярными связями (например, кремнезем SiO2), структурной единицей является условная формульная единица, в которой индексы у символов химических элементов отражают соотношение их количеств в кристалле.
Образец любого вещества можно охарактеризовать с помощью трех физических величин – массы m, объема V и количества вещества n.
Количество вещества – это число структурных единиц, составляющих данный образец веществf. Единицей измерения количества вещества является моль – это порция вещества, содержащая столько структурных единиц, сколько содержится атомов в 12 г изотопа углерода 12С. Последняя величина называется постоянной Авогадро NА (NА = 6,022 · 1023 моль-1).
Любые газы при одинаковых условиях (фиксированы температура и давление) имеют одинаковый молярный объем ( Vm = 22,4 дм3 /моль = 22,4 л /моль)
Химическая формула отражает качественный и количественный состав структурной единицы простого или сложного вещества.
Расчеты по схемам химических реакций:
Масса вступивших в реакцию реагентов равна массе образовавшихся продуктов. Таким образом, все вычисления по схеме реакции основаны на составлении уравнений материального баланса по количеству вещества или массе каждого элемента с последующим использованием соотношений, связывающих количество данных атомов с количеством вещества реагентов и продуктов реакции, в составе которых они находятся.
Расчеты по уравнениям химических реакций:
С помощью стехиометрических коэффициентов схема химической реакции переходит в ее уравнение, которое в явном виде отражает закон сохранения количества атомов каждого вида при переходе от исходных веществ (реагентов) к продуктам реакции. Стехиометрические коэффициенты позволяют установить связь между количествами участвующих в реакции веществ на основе следующего правила: коэффициенты в химическом уравнении задают молярные пропорции (отношения), в которых вступают в реакцию исходные вещества (реагенты) и образуются продукты реакции.
Пример: реакция синтеза аммиака: 3H2 + N2 = 2NH3
n (H2 ): n (N2 ): n (NH3 ) = 3:1: 2,
Отсюда n (NH3 ) = 2/3 n (H2 ) или n (NH3 ) = 1/2 n (N2 )
Газовые законы:
В основе расчета количества вещества, плотности и молярной концентрации газообразных веществ и их смесей при заданных давлении Р и температуре Т лежит уравнение Менделеева – Клапейрона (уравнение состояния идеального газа):
РV = nRT, которое можно представить в других формах:
Р = (n/V)/ RT = сRT или РV = m/M = RT,
где m – масса; М – молярная масса; с – молярная концентрация газа при данных Р и Т, где размерность физических величин зависит от выбранной системы единиц.
Справочно: 1 атм = 760 мм рт.ст. = 101325 Па = 101,325 кПа и Т [K] = 273 + t °C.
R= 8,314 Дж / (моль ˑ К), или 0,082 (л ˑ атм)/ (моль ˑ К)
Следствия из уравнения Менделеева – Клапейрона:
а) Закон Авогадро: при одинаковых условиях (Р, Т – фиксированы) равные объемы газов содержат одинаковое число молекул: если для двух газов V1 = V2, то n1 = n2, и наоборот.
б) Молярные объемы Vm любых газов при одинаковых условиях одинаковы, то есть при n = 1 моль, получаем Vm = RT/P
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ:1. Рассчитайте количество, массовые доли и массы химических элементов в 3,42 г сульфата алюминия Al2(SO4)3 .
Решение:
_____________________________________
_____________________________________
2. В какой массе меди содержится 10,0 г электронов? (Аr(е) = 0,0005486). (Ответ: 39942,4 г.)
Решение:
_____________________________________
_____________________________________
3. Содержание кремния и кислорода в земной коре составляет 27,6 % и 47,2 % по массе. Каких атомов, кремния или кислорода, больше в земной коре и во сколько раз? Какая доля кислорода связана с кремнием в виде оксида? (Ответ: соотношение 1: 3.)
Решение:
_____________________________________
_____________________________________
4. Запишите химические формулы минералов через условные формулы составляющих их оксидов: тальк – Mg3H2Si4O12 (например, 3MgO·4SiO2·H2O); мусковит – K2H4Al6Si6O24; нефелин – Na2Al2Si2O8; берилл – Be3Al2Si6O18.
Решение:
_____________________________________
_____________________________________
5. В асбесте содержатся элементы (по массе): 9,6 % Са; 17,3 % Mg; 26,9 % Si, остальное – кислород. Определите формулу минерала и запишите ее через формулы составляющих его оксидов.
Решение:
_____________________________________
_____________________________________
6. Минерал изумруд содержит по массе: 5 % Be; 10 % Al; 31 % Si и 54 % О, а также примесь хрома (III), придающую ему зеленую окраску. Определите формулу минерала и запишите ее через формулы составляющих его оксидов.
Решение:
_____________________________________
_____________________________________
7. При взаимодействии 7,1 г оксида фосфора(V) с избытком раствора гидроксида натрия получили 164 г раствора средней соли. Вычислите массовую долю соли в полученном растворе.
Решение:
_____________________________________
_____________________________________
8. При взаимодействии избытка карбоната магния со 146 г раствора хлороводорода было получено 2,24 л углекислого газа (н.у.). Вычислите массовую долю хлороводорода в исходном растворе.
Решение:
_____________________________________
_____________________________________
9. После пропускания 4,4 г углекислого газа через 320 г раствора гидроксида калия получили раствор средней соли. Вычислите массовую долю щёлочи в исходном растворе.
Решение:
_____________________________________
_____________________________________
10. К раствору хлорида железа(II) с массовой долей 5% добавили избыток раствора гидроксида натрия. В результате реакции образовался осадок массой 4,5г. Определите массу исходного раствора соли.
Решение:
_____________________________________
_____________________________________
11. Через 80 г раствора гидроксида натрия с массовой долей растворённого вещества 10% пропустили углекислый газ до образования карбоната натрия. Вычислите объём (н.у.), затраченного на реакцию газа.
12. Определите объём (н.у.) аммиака, который полностью прореагировал с раствором азотной кислоты массой 25,2 г и массовой долей кислоты 20%.
13. К 80 г раствора хлорида бария с массовой долей растворённого вещества 6,5% добавили избыток раствора серной кислоты. Вычислите массу выпавшего осадка.
14. В 73 г соляной кислоты с массовой долей HCl 5% поместили избыток цинка. Вычислите объём выделившегося газа (н.у.).
15. При анализе руды, содержащей халькозин Cu2S, установлено, что в 5,0 г ее содержится 2,7 г меди. Определите массовую долю примесей в руде. ( Ответ: 32,4 %.)
16. Определите массовую долю карбоната кальция в образце природного мрамора, если при термическом разложении его навески 7,85 г выделилось 1,52 л углекислого газа (н.у.). (Ответ: 86,6 %.)
17. Газ, образующийся при термическом разложении 44 г минерала, содержащего малахит (CuOH)2CO3 и примесь CuO, был поглощен известковой водой, образовавшийся осадок отделили и прокалили до полного разложения, при этом масса твердого остатка составила 8,4 г. Определите массовую долю примеси в минерале. (Ответ: 25 %.)
18. Массовая доля бурого железняка 2Fe2O3 . 3H2O в руде составляет 85 %. Определите массу руды, необходимую для получения 1 т железа, если степень его извлечения из руды 95 %. (Ответ: 2,07 т.)
19. При обжиге 10 т смеси пирита FeS2 и халькопирита СuFeS2 образовалось 3468 м3 газа (н.у.). Определите массовую долю меди в смеси. (Ответ: 7,1 %.)
20. Газообразные продукты полного термического разложения 97,2 г образца, состоящего из смеси минералов доломита CaCO3·MgCO3 и магнезита MgCO3, поглощают известковой водой, и при этом образуется 55,0 г карбоната и 44,6 г гидрокарбоната кальция. Определите массовые доли минералов в образце. (Ответ: доломит 56,8 %.)
21. При горении 3,84 г органического вещества было получено 2,12 г карбоната натрия, 2,24 л углекислого газа (н.у.) и 1,8 г воды. Установите формулу исходного вещества. (Ответ: пропионат натрия.)
22. При прокаливании 25,4 г смеси гидроксидов меди и алюминия масса образца уменьшилась на 28,35 %. Определить количества и массы веществ в исходной смеси. (Ответ: 0,1 моль; 0,2 моль.)
23. Смесь хлоридов натрия и кальция массой 24,78 г растворили в воде и в полученный раствор добавили избыток раствора нитрата серебра, и при этом выпал осадок массой 63,14 г. Определить количества и массы веществ в исходной смеси. (Ответ: 0,12 моль; 0,16 моль.)
24. Для хлорирования 12,0 г смеси стружек железа и меди потребовалось 5,6 л хлора (н.у.), и при этом образовалась смесь хлоридов железа (III) и меди (II). Определить количества и массы веществ в исходной смеси. (Ответ: 0,1 моль; 0,1 моль).
25. Массовые доли компонентов газовой смеси равны (в %): Cl2–67; Br2–28; O2–5;
вычислите: 1) объемные доли компонентов; 2) парциальные давления компонентов; 3) объем 1 кг смеси.
Общее давление равно 1,013 · 105 Па. Температура 373 К.
(Ответ: Cl2 (74 об.%, p = 0,750·105 Па); Br2 (13,7 об.%, p = 0,139 105 Па); O2 ( 12,2 об.%, p =0,124 ·105 Па.)
Часть 2. Практическая работа
ЗАДАНИЕ 1Предельно допустимые концентрации (ПДК) некоторых вредных веществ в атмосферном воздухе населенных пунктов, установленные в Российской Федерации (МР – максимальная разовая, СС – среднесуточная; класс опасности – чрезвычайно опасный – 1, малоопасный – 4):
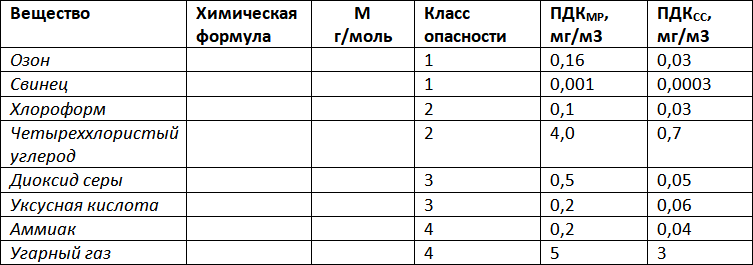
1. Запишите молекулярные формулы представленных химических соединений. Рассчитайте их молярные массы.
2. Укажите химическую природу веществ: органические/неорганические
3. Составьте графические формулы представленных соединений
4. Ответьте на вопросы, представив расчеты:
А) Какая допустимая максимальная разовая концентрация хлороформа будет создания в помещении, где проводится введение лабораторных животных в наркоз, если учесть, что объем лаборатории 55 м3
Б) Какая допустимая среднесуточная концентрация угарного газа может присутствовать в гаражном боксе, где находится автомобиль, если учесть, что объем бокса 40 м3
5. Предложите методы идентификации и количественного определения в воздухе аммиака, уксусной кислоты и свинца.
ЗАДАНИЕ 2Растворимость газов в водеРастворение в жидкостях даже достаточно больших объёмов газов не приводит к существенному росту объёма раствора по сравнению с объёмом взятого растворителя и при решении задач можно с хорошей точностью принять, что объём раствора равен объёму растворителя. Кроме того, говоря о растворимости газов в воде и других жидкостях, нужно помнить, что это характеристика насыщенного раствора данного газа и она зависит от его химической природы, температуры и парциального давления над раствором. При повышении температуры жидкости растворимость газов в ней падает, поэтому, например, удаление газов из воды достигается её кипячением. С другой стороны, рост парциального давления приводит к увеличению растворимости.
Химическая природа газа проявляется в том, что одни имеют аномально большую растворимость в воде, например, аммиак, галогенводороды, а другие образуют очень разбавленные растворы. К последним относятся газы, которые химически не взаимодействуют с водой – водород, азот, кислород, инертные газы, угарный и углекислый газы, газообразные углеводороды и др. Их растворимость при постоянной температуре описывается законом Генри:
p = KГ · x,
где p – парциальное давление растворенного компонента над раствором, x – его мольная доля в насыщенном растворе, KГ – константа Генри, имеющая размерность давления – Па, атм или мм рт.ст.
При расчете растворимости газов в воде закон Генри представляют в более удобном виде:
c = KГ* · p, где c – молярная концентрация газа в насыщенном растворе (моль/дм3 ), p – парциальное давление газа над раствором, KГ* – константа Генри, имеющая размерность моль / (дм3 ·давление).
Проведем пересчет констант Генри KГ, Па (из справочника) в KГ*, моль / (дм3 ·атм). Поскольку 1 атм = 101325 Па, то пересчет KГ, атм = KГ, Па / 101325
Данные таблицы соответствуют температуре 298 К = 25 °С:
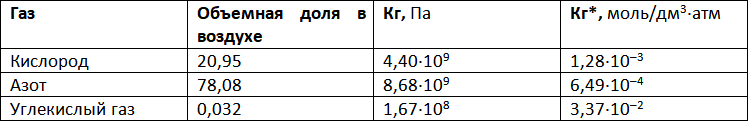
Задание: рассчитайте растворимость указанных компонентов воздуха в воде при 25 °С
Пример:
c = KГ* · p
с(О2) = 1,28·10–3 · 1 · 0,2095 = 2,682·10–4 моль/дм3 = 6,55 мл/дм3
Расчет для азота – N2:_____________________________________
Расчет для угарного газа – CO_____________________________________
Часть 3. Домашнеее задание
1. Сформулируйте определения понятий валентность, химическая связь, степень окисления. В чем разница между ними?
2. Назовите основные положения теории химического строения Бутлерова.
3. Что такое ионная связь? Почему её называют научной абстракцией?
4. Какая связь называется ковалентной? В чём разница между ковалентной полярной и неполярной связью? Что такое диполь?
5. Объясните чем σ-связь отличается от π-связи. Какие существуют механизмы образования общей электронной пары?
6. Какая связь называется металлической? Что у неё общего и различного с ковалентной связью?
7. Что называют силами Ван-дер-Ваальса? Какую связь называют водородной? В каких веществах она встречается?
8. Минерал альбит (натриевый полевой шпат) содержит по массе 32,1 % Si; 48,8 % О; остальное Al и Na. Определите формулу минерала и запишите ее через формулы составляющих его оксидов (при решении использовать условие электронейтральности).
9. Минерал берилл содержит по массе 31,285 % Si; 53,631 % О, а также Аl и Ве. Определите формулу минерала и запишите ее через формулы составляющих его оксидов (при решении использовать условие электронейтральности).
10. Вычислите объём аммиака (н.у.), необходимого для полной нейтрализации соляной кислоты массой 146 г и массовой долей HCl 10%.
11. Вычислите массу раствора азотной кислоты с массовой долей 15%, необходимой для полной нейтрализации раствора, содержащего 3,7 г гидроксида кальция.
12. В результате взаимодействия растворов нитрата серебра и хлорида калия, взятого в избытке, выпал осадок массой 2,87 г. Вычислите массу исходного раствора нитрата серебра с массовой долей 17%, взятого для реакции.
13. Вычислите объём углекислого газа, который был поглощён 740 г
0,2%-ного раствора гидроксида кальция, если после окончания реакции был получен прозрачный раствор гидрокарбоната кальция (Ca(HCO3)2).
14. Образец лунного грунта содержит по массе 16,2 % Са; 22,5 % Fe, а также кремний и кислород. При обработке 5,00 г этого образца при нагревании плавиковой кислотой выделилось 0,896 л тетрафторида кремния SiF4 (н.у.). Установите химическую формулу лунного минерала. (Ответ: CaFeSi2O6.
15. Прокалили 15,54 г неизвестной соли, в которой массовая доля кислорода ω(О) = 36 %, при этом образовалось 1,26 г воды, 1,568 л углекислого газа (н.у.) и оксид металла (II). Установите формулу соли. (Ответ: гидроксикарбонат меди – малахит.)
16. При сжигании 2,0 г смеси серы и угля образовалось 6,0 г смеси оксидов. Определить количества и массы веществ в исходной смеси. (Ответ: 0,1 моль ; 0,025 моль.)
17. Смесь гидроксидов бария и натрия массой 6,33 г полностью нейтрализовали раствором фосфорной кислоты, и образовалось 7,65 г смеси средних солей. Определить количества и массы веществ в исходной смеси. (Ответ: 0,03 моль; 0,03 моль.)
18. Смесь порошков алюминия и карбоната натрия массой 18,7 г обработали избытком соляной кислоты, и при этом образовалось 12,32 л газов (н.у.). Определить количества и массы веществ в исходной смеси. (Ответ: 0,3моль; 0,1 моль.)
19. Сплав натрия и калия массой 8,5 г обработали избытком воды, и при этом выделилось 3,36 л газа (н.у.). Определить количества и массы веществ в исходной смеси. (Ответ: 0,2 моль; 0,1 моль.)
20. Для уксусной кислоты ПДКМР = 0,2 мг/м3 . На складе разбили бутыль с кислотой, и в воздухе склада установилось парциальное давление её паров, равное 3 Па. Во сколько раз превышена ПДКМР? Внешние условия: давление 101,325 кПа, температура 298 К. (Ответ: в 370 раз.)
21. Сколько молекул формальдегида присутствует в см3 воздуха, если концентрация токсиканта соответствует ПДКМР = 0,035 мг/м3? (Ответ: 7,0 · 1011 1/см3 .)
22. Константы Генри KГ для кислорода и азота при 0° С равны 2,54·109 и 5,45·109 Па соответственно. Рассчитайте растворимость этих газов при н.у. (1 атм, 0 °С) и сравните её с растворимостью при стандартных условиях (1 атм, 25 °С). (Ответ: при н.у. с(О2) = 4,65 · 10–4 моль/дм3 = 10,42 мл/дм3 )
1.3. Использование качественного и количественного анализа химических соединений в медицинской практике
Часть 1. Лабораторная работа
«Основы качественного химического анализа органических веществ на примере производных 5-нитрофурана»
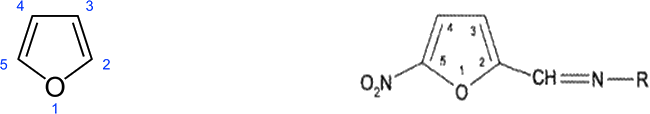
Фуран – ароматический гетероцикл, содержащий в качестве гетероатома атом кислорода. Синтетические производные нитрофурана (точнее – 5-нитрофурфурола, карбонильного производного фурана) обладают бактерицидным действием и используются как антибактериальные средства.
Производные 5-нитрофурана являются веществами кислотного характера. Кислотные свойства лекарственных веществ группы 5-нитрофурана проявляются в следующих видах взаимодействия:
• с водными растворами щелочей;
• с ионами тяжелых металлов
Фурацилин при использовании разбавленных растворов щелочей образует соль, окрашенную в оранжево – красный цвет.
При нагревании фурацилина в растворах гидрооксидов щелочных металлов происходит разрыв фуранового цикла и образуется карбонат натрия, гидразин и аммиак. Последний обнаруживают по изменению окраски влажной лакмусовой бумаги.
Раствор фуразолидона в тех же условиях, но при нагревании, приобретает красно – бурое окрашивание за счет разрыва лактонного цикла и образования соли:
Эта реакция может быть использована для отличия фурацилина от фурадонина и фурозолидона.
Фурадонин в разбавленных растворах щелочей при комнатной температуре образует в результате таутомерных превращений остатка гидантоина соль, окрашенную в темно – красный цвет.
ПРОТОКОЛ ОФОРМЛЕНИЯ ЛАБОРАТОРНОЙ РАБОТЫДата ______________________