Проектирование медицинских изделий
Важным аспектом здесь является тот факт, что изделие необходимо будет верифицировать или валидировать по некоторым критериям. Необходимо выбрать эти критерии, а также разработать и утвердить протокол оценки. В процессе проектирования эта процедура будет использоваться и тестироваться много раз, так как она является основой проверки соответствия проекта. Кстати, под эту процедуру подпадают клинические испытания и т. д. Также стоит отметить, что окончательная оценка, верификации и валидация будут указаны в исходной спецификации дизайна продукта.
4.7.4 Изменения дизайна
Эта процедура требуется для соответствия ISO 13485 7.3.9. По сути, у него две основные цели: во-первых, чтобы убедиться, что изменения дизайна значимы для функциональных, эксплуатационных требований, требований удобства пользования, безопасности и применимых нормативных требований в отношении изделия и его предусмотренного применения, во-вторых, чтобы гарантировать, что любые изменения осуществляются правильно, то есть включают оценку влияния изменений на составные части, полуфабрикаты или уже поставленную продукцию, на входные или выходные данные менеджмента риска и процессы жизненного цикла продукции.
Неудивительно, что изменение дизайна похоже на полностью новый дизайн продукта. Однако есть два основных отличия. Во-первых, эта процедура всегда будет относиться к существующему файлу проекта, поэтому первым шагом является открытие существующего файла. Эта процедура предназначена только для документации – она предназначена для правильного внесения изменений. Следовательно, приняв изменение, нужно убедиться, что оценены риски, связанные с указанным изменением. Конец (выход) процедуры отличается; здесь нужно убедиться, что изменение (или изменения) полностью задокументировано в файле, а старые документы сохранены в репозитории (рисунок 4.9).
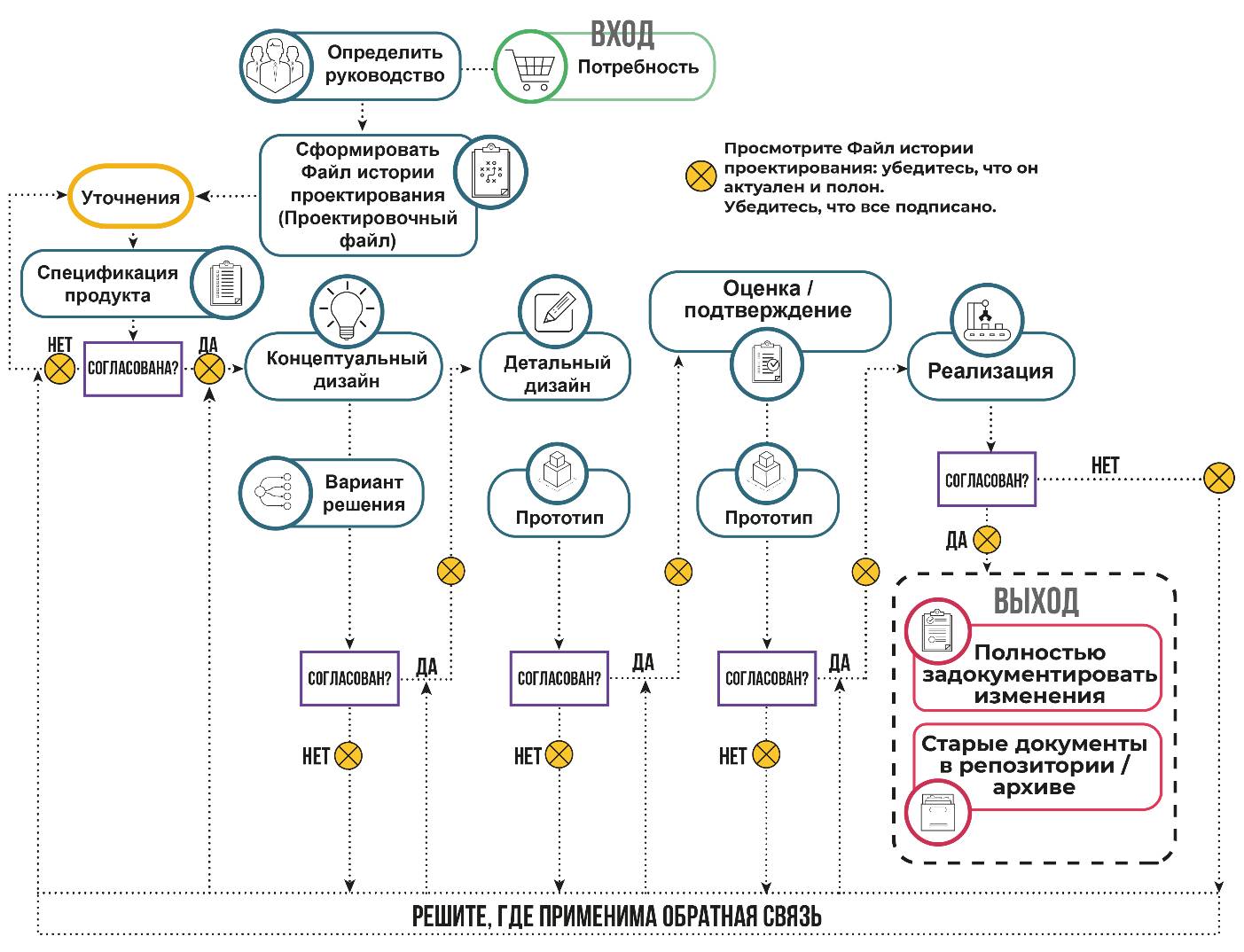
Рисунок 4.9 – Процедура изменения дизайна
Отметим, что некоторые изменения в проекте можно отслеживать внутри; в отношении других необходимо будет информировать регулирующие органы.
4.7.5 Управление документами
Очень важно иметь документооборот, которым необходимо управлять. Записи – особый вид документов, и ими надо управлять согласно требованиям, приведенным в пункте 4.2.5 ISO 13485. Компания должна обеспечивать анализ и официальное одобрение изменений в документах либо должностным лицом, одобрившим первоначальный документ, либо другим специально назначенным должностным лицом, имеющим доступ к соответствующей исходной информации, на основании которой принимается решение. Также должен быть определен период времени, в течение которого следует хранить не менее одной копии устаревших документов. На этот период должен быть обеспечен доступ к документам, в соответствии с которыми медицинское изделие было изготовлено и испытано, в течение, по крайней мере, срока службы изделия, определенного организацией, но не менее срока хранения любой итоговой записи или в соответствии с применимыми нормативными требованиями.
4.7.6 Процедура оценки риска
Проведение оценки рисков при принятии решения является хорошей практикой. Это заставляет проверять последствия решений. Предположим, например, что компания решила заменить один компонент в большом изделии. Изменение может быть безобидным, например, уменьшение диаметра штифта, удерживающего экран на месте. Однако это изменение теперь делает все продаваемые предыдущие устройства разными – как вы гарантируете, что если кто-то попросит сменный штифт, он получит правильный размер? Каков риск (или риски), если они получат неправильный размер? Поскольку это так важно, у него есть собственный стандарт – ISO 14971 «Изделия медицинские. Применение менеджмента риска к медицинским изделиям», который рассмотрим в следующей главе. Он должен быть адаптирован к конкретным обстоятельствам, в которых он будет использоваться, однако это применимая процедуры.
Важной частью этой процедуры является заполнение утвержденной формы. Без этого вся процедура не получится. Как и в случае с предыдущими процедурами, важно документировать анализ на ключевых этапах (и, конечно же, файл). Также важно убедиться, что любые действия, предложенные в результате анализа рисков, действительно предприняты и зарегистрированы.
РЕЗЮМЕ
В этой главе в качестве основы для процедур проектирования мы рассмотрели рекомендации стандарта ISO 13485 (и семейство ISO 9000). Важно, что нормативы по медицинским изделиям требуют одного – правильного выполнения проектной деятельности. Стандарт устанавливает требования к системе менеджмента качества в случаях, когда организации необходимо продемонстрировать способность поставлять медицинские изделия и предоставлять связанное с ними обслуживание, отвечающие требованиям потребителя и применимым регулирующим требованиям. Такие организации могут быть вовлечены в одну или несколько стадий жизненного цикла медицинского изделия, включая проектирование и разработку, производство, хранение и дистрибуцию, монтаж и обслуживание, а также проектирование и разработку или оказание связанных с медицинскими изделиями услуг (например, технического обслуживания).
В этой главе мы познакомились с процедурами проектирования и увидели, как процедуры используются для демонстрации соответствия требованиям стандарта ISO 13485 по контролю за проектированием и как они используются для обеспечения правильной разработки изделия с первого раза. Далее мы увидели, что компания должна документировать процедуры проектирования и разработки. Несмотря на то, что была предпринята попытка предоставить процедуры, которые носят общий характер, важно, чтобы были разработаны собственные процедуры, поскольку это поможет полностью понять компанию, линейку продуктов и клиентов.

1. Опишите фазы жизненного цикла медицинского изделия для диагностики in vitro на примере теста для выявления вируса гепатита А в крови.
2. Чем процедура изменения дизайна изделия отличается от процедуры разработки нового изделия?
3. Какие вопросы важны для определения потребности в изделии?
4. Является ли процедура аудита/обзора изделия постоянной процедурой?
5. Укажите основные цели аудита процессов проектирования изделия.


1. ГОСТ ISO 13485-2017 "Изделия медицинские. Системы менеджмента качества. Требования для целей регулирования"
2. Kheir O, Smedts S, Jacoby A, Verwulgen S. Efficient Quality Management in MedTech Start- Ups (Based on ISO 13485). Med Devices (Auckl). 2021 Oct 15;14:313-319. doi: 10.2147/ MDER.S320583. PMID: 34703329; PMCID: PMC8526944.
3. Linders PWJ. Setting Standards: ISO 13485: Challenges in Achieving High-Level Structure Compliance. Biomed Instrum Technol. 2020 Jan./Feb.;54(1):68-70. doi: 10.2345/0899-8205-
54.1.68. PMID: 31961738.
4. Ward A. ANSI/AAMI/ISO 13485 comes of age. Biomed Instrum Technol. 2007 Mar- Apr;41(2):145-6. doi: 10.2345/0899-8205(2007)41[145:ICOA]2.0.CO;2. PMID: 17432668.

5 Проектирование медицинских изделий с учетом эксплуатационной пригодности
Безопасность медицинских изделий зависит от их использования по назначению, а также от надежности. Соответственно требуется, чтобы разработчики, которые занимается проектированием и оценкой медицинских изделий, учитывали человеческий фактор в своих процессах. Проще говоря, «человеческий фактор» относится к тому, как человек будет взаимодействовать с окружающими его системами, включая технологии, которые он использует. Во многом это взаимодействие будет зависеть от конструкции изделия, от того, какое образование и какую подготовку имеет пользователь, а также от среды, в которой он будет использовать технологию. Научная дисциплина человеческого фактора использует знания из самых разнообразных областей, таких как анатомия, психология, инженерия и физиология, чтобы помочь разработать продукты, которые подходят пользователю для более эффективного и безопасного применения. Человеческий фактор учитывает особенности целевой группы пользователей, такие как возраст, размер, сила, когнитивные способности и уровень подготовки. Кроме того, он принимает во внимание предполагаемую среду использования: больничные палаты, отделения интенсивной терапии, машины скорой помощи или домашние условия. Также учитываются потенциальные конкурирующие отвлекающие факторы, например, уровень освещения или срочность использования.
Принципы человеческого фактора в течение многих лет применялись в отраслях с высокой степенью опасности, таких как оборонная, ядерная, нефтехимическая и транспортная, чтобы минимизировать риски, связанные с ошибками при использовании, и продвигать безопасные методы, а также использовать преимущества технологий, которые предвосхищают и уменьшают количество ошибок при их использовании.
Термин «человеческий фактор» включает в себя и такие термины, как эргономика и удобство использования. Процесс создания пригодных для использования продуктов, отвечающих потребностям пользователей и соответствующих их практике, часто называют «проектированием удобства использования».
В этой главе говорится о том, что проектирование удобства использования – это повторяющийся процесс, включающий проектирование, тестирование и проверку этапов проектирования, а также требует внимания к постпродажной фазе, поскольку во время использования изделия в клинической практике могут появиться доказательства того, что конструкция требует дальнейшего улучшения.
5.1 Термины и определения
Нормальная эксплуатация/применение – применение, включая текущий осмотр и регулировку любым пользователем, включая функционирование в режиме ожидания, в соответствии с инструкциями по эксплуатации или в соответствии с общепринятой практикой применения медицинских изделий, к которым не предоставляются инструкции по эксплуатации.
Примечания к определению:
1. Нормальную эксплуатацию/применение не следует путать с предусмотренным применением/назначением. Хотя оба понятия включают в себя концепцию применения по назначению изготовителя, предусмотренное применение/назначение сфокусировано на медицинской цели, тогда как нормальная эксплуатация включает в себя не только медицинскую цель, но и техническое обслуживание, транспортирование и т.д.
2. При нормальной эксплуатации могут возникать ошибки эксплуатации/применения.
3. В некоторых юрисдикциях медицинские изделия, которые могут быть безопасно использованы без инструкции по эксплуатации, освобождены от необходимости иметь инструкцию по эксплуатации.
Ненормальная эксплуатация/применение – сознательное, преднамеренное действие или преднамеренное бездействие, которое противоречит или нарушает нормальную эксплуатацию/ применение, находящуюся за пределами принятия изготовителем всех дальнейших рациональных мер по управлению риском, связанным с пользовательским интерфейсом. Пример – небрежное применение, саботаж или преднамеренное игнорирование информации по безопасности.
Правильная эксплуатация/применение – нормальная эксплуатация без ошибок эксплуатации/применения.
Примечание к определению:
Отклонение от инструкций по эксплуатации считается ошибкой применения только в том случае, если оно приводит к такому отклику медицинского изделия, который отличается от предусмотренного изготовителем или от ожидаемого пользователем.
Проектирование с учетом эксплуатационной пригодности/человеческого фактора – применение знаний о поведении человека, его возможностях, ограничениях и о других его характеристиках к проектированию медицинского изделия (включая программное обеспечение), систем и задач для достижения достаточной эксплуатационной пригодности.
Достижение достаточной эксплуатационной пригодности может обеспечить допустимый уровень риска, связанный с применением.
Ошибка эксплуатации/применения – выполнение или невыполнение пользователем действия при использовании медицинского изделия, приводящее к такому результату его функционирования, который отличается от предусмотренного изготовителем или ожидаемого пользователем.
Примечания к определению:
1. К ошибкам эксплуатации/применения относят неспособность пользователя завершить задачу.
2. Ошибки эксплуатации/применения могут быть вызваны несоответствием между характеристиками пользователя, пользовательского интерфейса, задачи или среды применения.
3. Пользователи могут осознавать или не осознавать, что произошла ошибка эксплуатации/ применения.
4. Неожиданную физиологическую реакцию пациента не относят к ошибке применения.
5. Неисправность медицинского изделия, которая приводит к неожиданному результату, не относят к ошибкам эксплуатации/применения.
Пользователь – лицо, взаимодействующее с медицинским изделием (то есть осуществляющее его эксплуатацию или обслуживание).
Примечания к определению:
1. У медицинского изделия может быть более одного пользователя.
2. Словосочетание «обычные пользователи» включает медицинских работников, пациентов, персонал, осуществляющий очистку, обслуживание, а также предоставляющий услуги.
Пользовательский интерфейс - средства, с помощью которых происходит взаимодействие пользователя и медицинского изделия.
Примечания к определению:
1. Сопроводительная документация считается частью медицинского изделия и его пользовательского интерфейса.
2. Пользовательский интерфейс включает все элементы медицинского изделия, с которыми взаимодействует пользователь, включая физические аспекты медицинского изделия, видео/ аудио/тактильные отображения, и не ограничивается программным интерфейсом.
Формирующее оценивание – оценивание пользовательского интерфейса, проведенное с целью рассмотрения сильных и слабых сторон проекта пользовательского интерфейса, а также непредвиденных ошибок эксплуатации/применения.
Примечание к определению:
Формирующее оценивание обычно выполняется итеративно на протяжении всех процессов проектирования и разработки, но до итогового оценивания, с целью обеспечения руководства разработкой пользовательского интерфейса по мере необходимости.
Итоговое оценивание – оценивание пользовательского интерфейса, проводимое на завершающей стадии разработки пользовательского интерфейса с целью получения объективных свидетельств того, что пользовательский интерфейс может быть использован безопасно.
Примечание к определению:
Итоговое оценивание относится к валидации безопасного использования пользовательского интерфейса.
Эксплуатационная пригодность – характеристика пользовательского интерфейса, которая облегчает использование и тем самым устанавливает результативность, эффективность и степень удовлетворенности пользователя в предусмотренной среде применения.
Примечание к определению:
Все аспекты эксплуатационной пригодности, включая результативность, эффективность и степень удовлетворенности пользователя, могут повышать или снижать уровень безопасности.
5.2 Человеческий фактор: почему он важен для безопасности пациентов
Все большее число медицинских изделий используется для диагностики и лечения пациентов, и ошибки в их использовании, приводящие к причинению вреда пациенту, вызывают особую обеспокоенность (рисунок 5.1). Такие ошибки могут быть связаны с ненадежной конструкцией изделия, особенно если речь идет о сложном пользовательском интерфейсе. Медицинские изделия, например инфузионные насосы, аппараты ИВЛ, автоматические электронные дефибрилляторы и изделия, включающие в себе лекарства (например, автоинъекторы), признаются потенциально имеющими проблемы с конструкцией, связанные с использованием. Они могут привести к таким проблемам, как передозировка, неправильная терапия и опасные задержки или трудности с доставкой лекарственных препаратов.
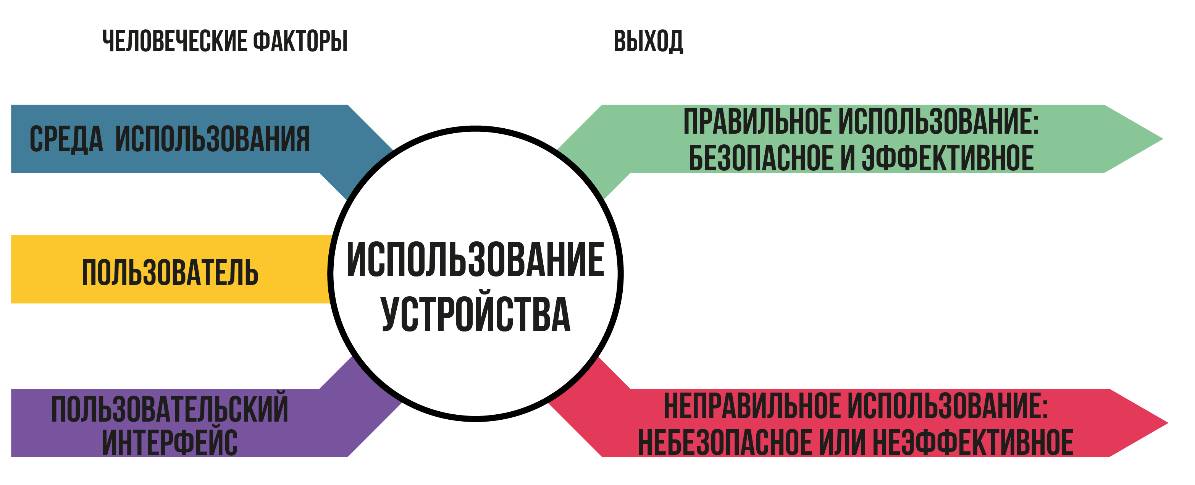
Рисунок 5.1 – Проектирование с учетом эксплуатационной пригодности/человеческого фактора приводит либо к безопасному и эффективному использованию, либо к небезопасному или неэффективному использованию. (Руководство FDA «Применение человеческого фактора и инженерии удобства использования к медицинским изделиям», февраль 2016 г)
По мере того, как медицинские изделия становятся все более разнообразными по своим возможностям, а среда, в которой они используются, все более сложной, с новыми отвлекающими факторами и требованиями к специализированному обучению, вероятность ошибки при использовании также увеличивается. Кроме того, по мере развития здравоохранения и переноса ухода за пациентами в домашнюю или общественную среду менее квалифицированные или даже неквалифицированные пользователи, включая пациентов и лица, осуществляющих уход, должны иметь возможность безопасно использовать довольно сложные медицинские изделия.
Процесс проектирования удобства использования может и должен осуществляться производителями изделий для идентификации, оценки и снижения потенциальных рисков для безопасности пациентов и пользователей; также при анализе произошедших инцидентов, чтобы определить обучение и принять корректирующие меры для улучшения конструкции изделия.
5.3 Нормативные требования по проектированию медицинских изделий с учетом эксплуатационной пригодности (человеческого фактора)
Поскольку инициативы по обеспечению безопасности пациентов играют все более важную роль в политике общественного здравоохранения, производителю требуется четко указать необходимость учета эргономического дизайна при разработке изделия.
Общие требования безопасности и эффективности медицинских изделий в странах ЕАЭС (Решение № 27) включают требования к человеческому фактору, которые выделены ниже.
– Медицинские изделия проектируются и изготовляются таким образом, чтобы при использовании в условиях и в целях, соответствующих их назначению, определенному производителем, и при необходимости с учетом технических знаний, опыта, образования или специальной подготовки, клинического и физического состояния пользователя они действовали согласно назначению, определенному производителем, и были безопасны для пользователя и третьих лиц при условии, что риск, связанный с их применением, является приемлемым при сопоставлении с пользой для пользователя (пункт 3).
– Решения, принятые производителем при проектировании и изготовлении медицинского изделия, должны соответствовать принципам безопасности с учетом общепризнанного уровня развития знаний. При необходимости производитель управляет рисками таким образом, чтобы остаточный риск, связанный с любой опасностью, являлся приемлемым. Производитель руководствуется следующим принципом в порядке приоритетности:
• выявление известной или прогнозируемой опасности и оценка связанных с ней рисков, возникающих при использовании медицинского изделия по назначению и при предсказуемом неправильном использовании (пункт 4).
– Для каждого медицинского изделия предоставляется информация, необходимая для идентификации этого медицинского изделия и его производителя, страны происхождения, а также информация для пользователя (профессионального или непрофессионального), касающаяся безопасности медицинского изделия, его функциональных свойств и эксплуатационных характеристик. Такая информация может находиться на самом медицинском изделии, на упаковке или в инструкции по применению (пункт 9).
Для медицинских изделий, применяемых в условиях воздействия внешних факторов также указано (пункт 28):
– Медицинские изделия проектируются и изготавливаются таким образом, чтобы устранить или снизить до приемлемого уровня:
1. риск травмирования пользователя или третьих лиц в связи с физическими характеристиками медицинского изделия;
2. риск ошибки при использовании медицинских изделий из-за конструктивных характеристик или человеческого фактора.
Для медицинских изделий для диагностики in vitro, применяемые в условиях воздействия внешних факторов указано (пункт 82) :
– Медицинские изделия для диагностики in vitro проектируются и изготавливаются таким образом, чтобы устранить или снизить до приемлемого уровня:
1. риск травмирования пользователя или третьих лиц в связи с физическими характеристиками медицинского изделия для диагностики in vitro;
2. риск ошибки при использовании медицинского изделия для диагностики in vitro из- за конструктивных характеристик или человеческого фактора.
Для медицинских изделий для диагностики in vitro, предназначенных для самотестирования пользователем или тестирования вблизи пользователя, указано:
– Медицинские изделия для диагностики in vitro, предназначенные для самотестирования пользователем или тестирования вблизи пользователя, проектируются и изготавливаются таким образом, чтобы максимально снизить риск ошибки пользователя, не имеющего специального медицинского образования, при применении таких медицинских изделий, а также при отборе проб или интерпретации результатов тестирования (пункт 103).
– Медицинские изделия для диагностики in vitro, предназначенные для самотестирования пользователем или для тестирования вблизи пользователя, должны иметь, если это объективно возможно, функцию подтверждения того, что при использовании эти медицинские изделия будут функционировать в соответствии с назначением, определенным производителем (пункт 104).
Кроме того, для тестов ИВД для самотестирования изготовитель должен иметь данные, свидетельствующие о пригодности изделия к обращению с учетом его предполагаемого назначения для самотестирования.
5.4 Процесс разработки эксплуатационной пригодности
Целями процесса разработки удобства эксплуатации являются изделия, которые просты в использовании и безопасны в предполагаемом контексте использования и предполагаемыми пользователями (будь то лица, осуществляющие уход, или сами пациенты). Пользователям не нужно читать, понимать и запоминать сложные инструкции и адаптировать их к требованиям изделия или применять его неудобным, неправильным и, возможно, опасным способом: хорошо спроектированное изделие просто в использовании и имеет пользовательский интерфейс, соответствующий пользовательскому опыту и ожиданиям.
Помимо соображений безопасности, изделия, разработанные с учетом принципов человеческого фактора, более приятны в использовании и, следовательно, могут привести к лучшему соблюдению правильной эксплуатации с требуемой частотой. Поэтому принципы человеческого фактора используются многими компаниями в дизайне для обеспечения лояльности клиентов и в маркетинговых целях.
Рисунок 5.2 описывает этапы типичного процесса, иллюстрируя его итеративный характер. Процесс должен быть зафиксирован в файле проектирования с учетом эксплуатационной пригодности. Заявления о соответствии стандарту МЭК 62366 недостаточно без подтверждающих доказательств. Файлы разработки эксплуатационной пригодности должны быть четкими и лаконичными, а документация должна быть подготовлена так, чтобы максимально упростить доступ ко всей необходимой информации заинтересованным лицам, например, экспертам.
В таблице 5.1 обобщены широко используемые методы разработки эксплуатационной пригодности, и они приведены в соответствие с этапами процесса разработки эксплуатационной пригодности (рисунок 5.2). Не все эти методы подходят для каждого процесса, и дополнительные методы могут применяться людьми с соответствующим опытом; список методов является иллюстративным, а не обязательным. Тем не менее пользовательское тестирование и анализ видов отказов и последствий (FMEA) обычно считаются минимальными требованиями.
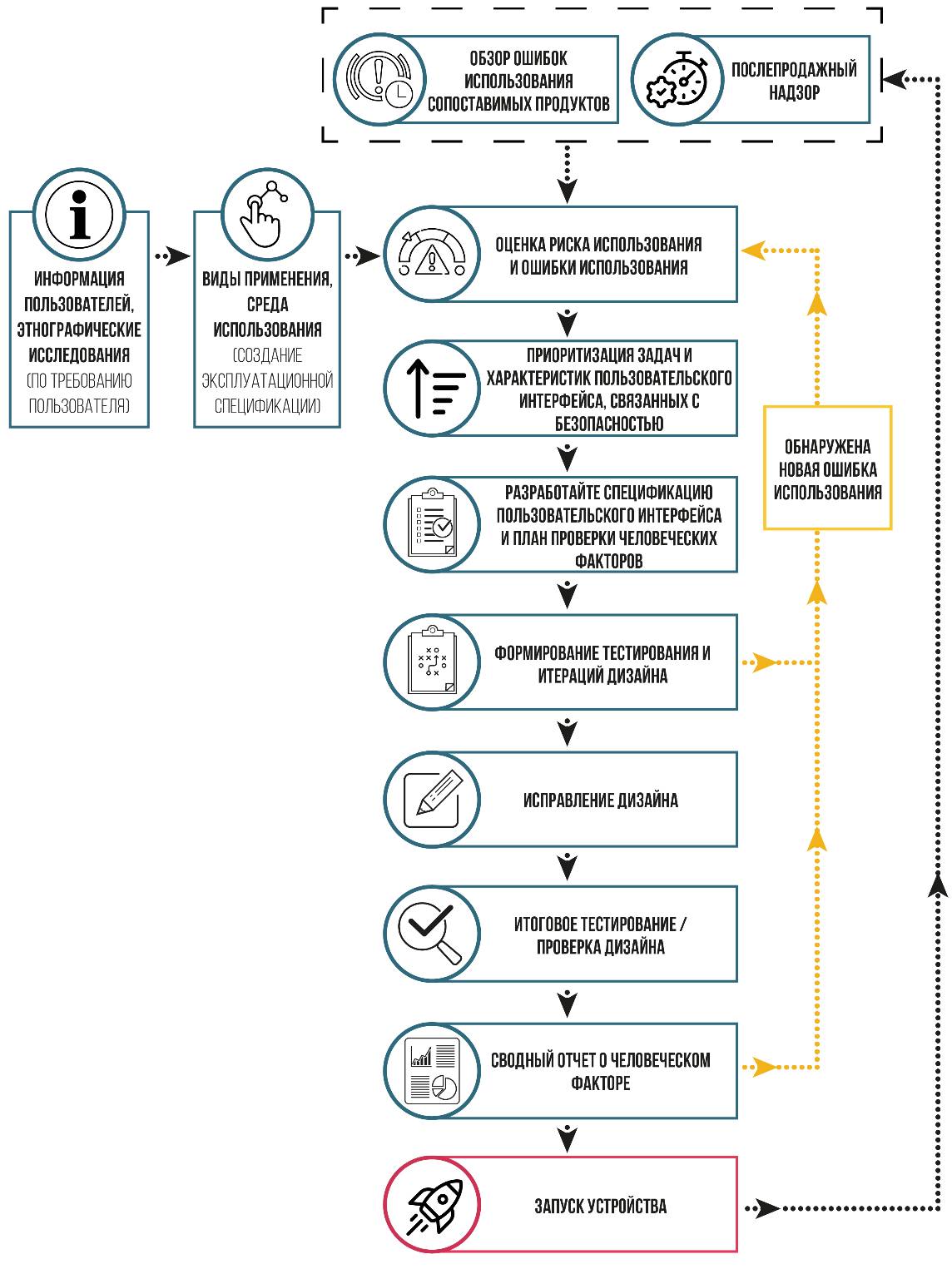
Рисунок 5.2 – Пример процесса проектирования с учетом эксплуатационной пригодности
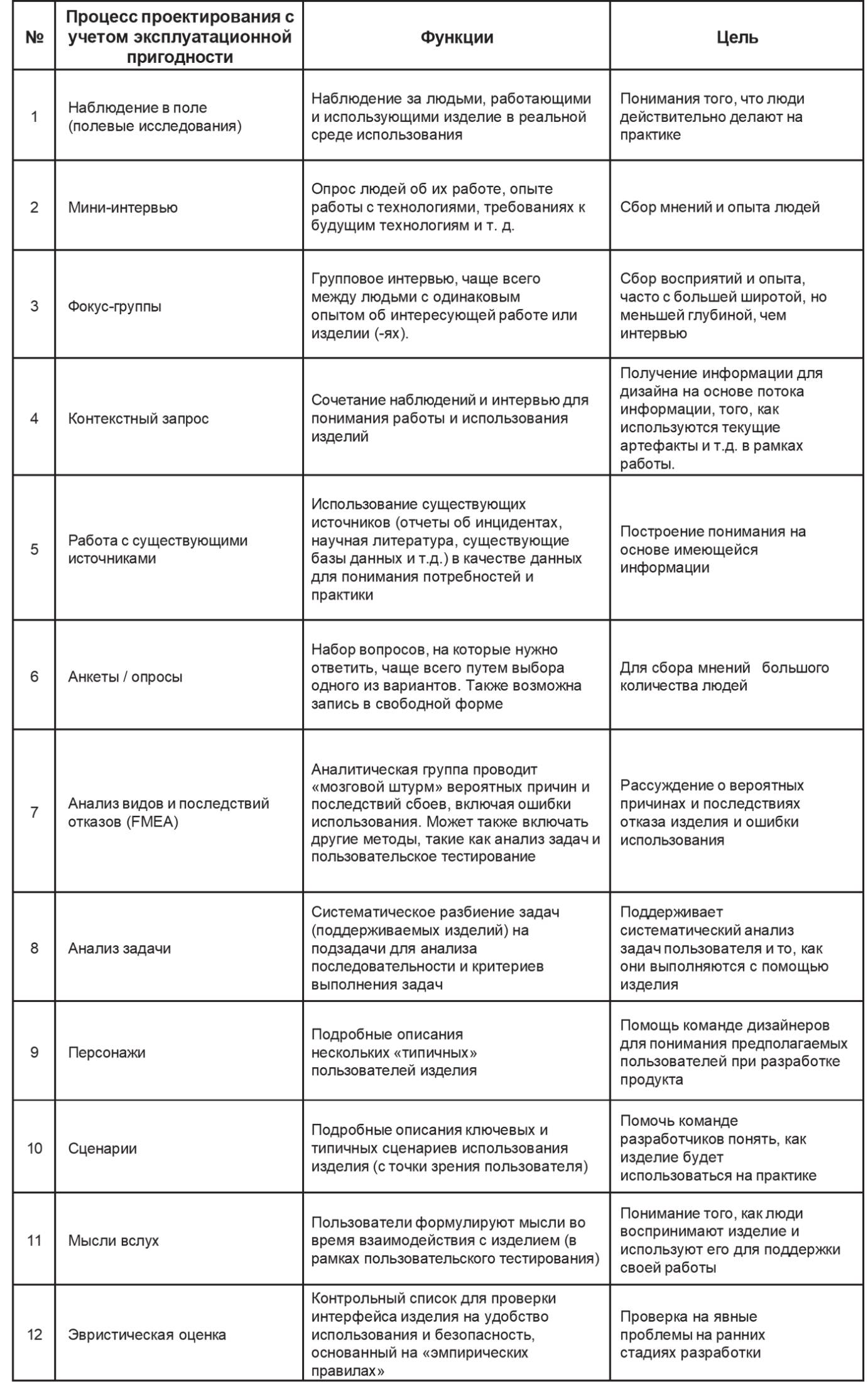
Таблица 5.1 – Основные характеристики проектирования с учетом эксплуатационной пригодности (человеческого фактора) для медицинских изделий
5.5 Этапы процесса проектирования медицинских изделий с учетом эксплуатационной пригодности (человеческого фактора)